今日は、commensal bacteria(共生細菌)が、腸腔内から腸管のLamina propria(粘膜固有層)に紛れ込んだりした時に、どのように対応するのかについて話しましょう。左下の絵を見ながら説明していきましょう。
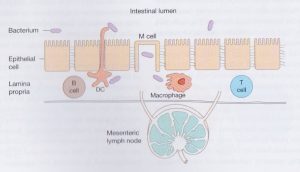 元来、共生細菌が腸管の粘液を突破して上皮細胞に引っ付いたとしても、上皮細胞を突破して、その下にある粘膜固有層に到達することは難しいのです。なぜかと言うと、左の絵を見ればわかるように、上皮細胞に共生細菌が近づいてくると、DCという樹状細胞が上皮細胞の中を突き抜けて枝を伸ばし、上皮細胞の近辺にいるバクテリアを捕まえていることがお分かりになるでしょう。このようにDCは、あちこちの上皮細胞を突き抜けて共生細菌を取り込もうとしているのです。さらにM cellを見てください。M cellはパイエル板にある細胞ですね。このパイエル板は小腸の末端である回盲部にたくさんあることはご存知ですね。
元来、共生細菌が腸管の粘液を突破して上皮細胞に引っ付いたとしても、上皮細胞を突破して、その下にある粘膜固有層に到達することは難しいのです。なぜかと言うと、左の絵を見ればわかるように、上皮細胞に共生細菌が近づいてくると、DCという樹状細胞が上皮細胞の中を突き抜けて枝を伸ばし、上皮細胞の近辺にいるバクテリアを捕まえていることがお分かりになるでしょう。このようにDCは、あちこちの上皮細胞を突き抜けて共生細菌を取り込もうとしているのです。さらにM cellを見てください。M cellはパイエル板にある細胞ですね。このパイエル板は小腸の末端である回盲部にたくさんあることはご存知ですね。
クローン病の人は、この回盲部のパイエル板のM細胞から取り入れられた異物である化学物質とキャリアタンパクが結びついた抗原がLamina propria(粘膜固有層)に取り込まれ、ここで前回述べたように“resident macrophage”(M2型マクロファージ)に貪食され、ここで炎症が起こり始めます。“resident macrophage”(M2型マクロファージ)で処理ができなくなると、血管にいる単球を呼び出し、この単球は活性化されM1型マクロファージになってさらに戦いが激しくなり、炎症が何回も繰り返されると、その部分のLamina propria(粘膜固有層)が破壊され、繊維化が起こり、最後は狭窄が生じ、食べたものが通らなくなったりして回盲部の腸管の一部を摘出するという手術を余儀なくされてしまうのです。
もちろんこのパイエル板は回盲部だけにあるのではなくて、小腸には200箇所もあるといわれています。従って、それぞれのパイエル板のM細胞から取り込まれた化学物質とキャリアタンパクが結びついた抗原がLamina propria(粘膜固有層)に取り込まれ、そこでLamina propria(粘膜固有層)において同じように炎症が起こり、その時に痛みが出たり、熱が出たり、最後は狭窄が起こって、その部分の切除をしなければならなくなるのです。
ところがさらに処理できないバクテリアは、DC(樹枝状細胞)によってリンパ管を流れて、絵の下に書かれている腸間膜にある非常に大事なリンパ節の一つであるMesenteric lymph node(腸間膜リンパ節)に運ばれていきます。そこで抗原提示細胞(APC)である樹枝状細胞は、運んできた抗原複合体や細菌やウイルスをナイーブT細胞(ヘルパー1T細胞やキラーT細胞)に提示して、活性化します。活性化した2種類のT細胞は血管を通って再び戦場であるLamina propria(粘膜固有層)に戻り、そこで敵と戦い始めます。と同時に、戦場にいる大食細胞はインターロイキン1(IL-1)やTNFαをどんどん産生します。すると、Lamina propria(粘膜固有層)に分布している毛細血管の血管内皮細胞がIL-1やTNFαを嗅ぎ付けます。すると毛細血管を超スピードで流れている好中球の細胞膜にひっついているセレクティン・リガンドと血管内皮細胞についているセレクティンが結びつくと、好中球の流れの速さがスローになります。
さらにLamina propria(粘膜固有層)の組織にいる補体(complement)も、敵である抗原(免疫複合体や細菌)に結びつくと、補体はC5aになります。CというのはComplementの略です。C5aは、ケモアトラクタントともいい、英語で“chemoattractant”といい、化学誘引物質と訳します。(補体についてはこちらを読んでください。)かつ組織にいる細菌は細胞膜の一つの成分であるLPSという分子を放出します。LPSはリポポリサッカライドといいます。日本語で脂質多糖類体と訳します。LPSやC5aが炎症性シグナルといいます。組織にこの炎症性シグナルであるLPSやC5aが増えると、このシグナルを毛細血管にある好中球が気づいて、好中球は蓄えておいたインテグリン(INT)という化学物質を好中球の細胞膜に運びます。このインテグリン(INT)は毛細血管の内細胞に常に表出されているICAMと結びつきます。ICAMというのは、“Inter cellular adhesion molecule”の略であり、日本語では「細胞間接着分子」と訳します。INTとICAMが結び付くと、毛細血管の好中球は結合した場所で走ることを止めてしまいます。ひとたび好中球が走ることをやめます。その間に組織には細菌のタンパクの破片であるN-ホルミルメチオニン(N-Formylmethionine)というペプチドです。N-Formylmethionineは略してfMetといいます。先ほど述べたC5aと同じくfMETはケモアトラクタントであり、血管から血管外へ好中球を運び出してくれるのです。好中球は血管外に出ると大食細胞が出すTNFαによって活性化され、敵である細菌などを貪食する力が増えるのです。
血管からLamina propria(粘膜固有層)という組織に、どのようにして好中球が出ていくのかを詳しくしたのは、実は私自身のためなのです。勉強というのは人のためにするのではなくて、深い真実を完全に自分が理解するためですね。真実を知りたい人は難しいですがついてきてください。
このようにして好中球も腸管のLamina propria(粘膜固有層)に出て戦いをした結果、腸管に炎症が起こり化膿したりして、化膿巣を除去するために手術する必要がある時があります。虫垂炎も同じ機序で起こるのです。虫垂炎もリンパ節であることはご存知ですね。
腸管というのは、常に悪玉菌も常在細菌として常に存在している上に、飲食物に含まれる様々な細菌が毎日毎日入ってくるわけですから、上に述べたような炎症が起こっていればたまりませんね。そこで腸管の免疫は特別なシステムが進化したのです。
炎症を起こす最初の細胞はマクロファージ(大食細胞)ですね。先週書いたように、マクロファージにはM1型とM2型の2つあることは書きましたね。そこで述べたように、腸管のマクロファージはM2型に属することは覚えてますか?元来、炎症を起こすのは、炎症細胞の代名詞にもなっている大食細胞であります。上の絵で示したように、大食細胞は血管から自分と同じ仲間の退職細胞や好中球を血管から戦場に集めますね。ところが既に述べたように腸管のLamina propria(粘膜固有層)のマクロファージは、炎症を起こさない“non-inflammatory maclophage”に進化したのです。様々な実験でもこの事実は証明されています。言い換えると、Lamina propria(粘膜固有層)のマクロファージは、敵を貪食する力は強いのでありますが、貪食した後、全面的な戦いをやったり、その結果炎症を起こすようなシグナルとなるサイトカインを放出しないということがわかっております。その結果、腸管の共生細菌がたまたまLamina propria(粘膜固有層)に漏れ出ても、継続して激しい戦いはしないということがわかっているのです。あるいは、Lamina propria(粘膜固有層)以外の他の組織では、激しい戦いをする病原性の強い細菌やウイルスとの戦いも炎症を起こさない温和な戦いであるということもわかっています。
それでは強力な病原体がきたときは、腸管の免疫はどのような戦いをするのでしょうか?例えば共生細菌にしろ病原性の強い細菌が大量に侵入した時に、危険な侵入者に対してどのように対処するのでしょうか?上で説明したように、腸管に強力な敵が侵入します。
すると樹状細胞は手を伸ばして捕まえたり、M細胞が捕まえたりしてLamina propria(粘膜固有層)にまで運び込みます。強力な的ですから、Lamina propria(粘膜固有層)にいる大食細胞や好中球だけでは処理できなければ、その敵を樹状細胞がLamina propria(粘膜固有層)の下にある腸間膜リンパ節に運ばれます。腸間膜リンパ節はリンパ節の中で一番大きくて立派だといわれます。抗原提示細胞(APC)である樹状細胞は、その細菌の敵の抗原を認識するヘルパー1T細胞(Th1)に提示します。そうすると、Th1細胞は活性化されます。活性化されたTh1細胞は、IFNγというサイトカインを分泌します。IFNγはLamina propria(粘膜固有層)にいるマクロファージの殺菌力を高めます。Th1は既に述べたように、インターロイキンを産生します。しかも腸管の上皮細胞は恒常的にTGFβというサイトカインを作っています。このIL-6とTGFβが、ナイーブT細胞をTh17細胞に変えます。このTh17という細胞は、腸管の免疫において極めて重要な仕事をしてくれます。このTh17細胞炎症を起こす力が極めて強いのです。というのはこのTh17細胞IL-17とIL-21とう2つのサイトカインを産生します。とりわけIL-17は、Lamina propria(粘膜固有層)の毛細血管から大量の好中球を血管外へ呼び寄せるのです。ちょうど上の説明でfMETとC5aというケモアトラクタント(化学誘引物資)が血管外へ好中球を呼び寄せるのと似ています。
ところがIL-17は、fMETやC5aよりもはるかに血管外へ好中球を呼び寄せる力が強いのです。さらにIL-17とIL-21というサイトカインは、腸管の上皮細胞どうしを結びつけているタイトジャンクション(密集結合)という働きを強めます。つまり密集結合とは、分子が通過できないようにする細胞間結合であります。Th17の出すサイトカインであるIL-17とIL-21の3つめの働きは、粘液の産生を高めます。4つめは、腸管の特徴的な抗体であるIgAがLamina propria(粘膜固有層)から腸管腔内へ上皮細胞を通って輸送されるのを促進します。これをトランスサイトーシス(transcytosis)といいます。この腸管腔内に輸送されたIgAは腸管腔内にいる細菌と結びついて、細菌と一緒に便として出されてしまいます。
次回はIgA抗体について詳しく書きます。
