中川恵一先生の「癌の秘密」というタイトルから間違いです。というのは癌には何も秘密がないからです。がんは最後に残った感染症であるワクチンが絶対に作ることができないヘルペス性慢性感染症であるからです。エジプト文明の時代からあったことが知られている癌はherpes感染症で死んだ帝王なのです。ピラミッドのお墓の棺桶に埋葬されていたミイラで発見された骨癌は実は骨に感染したherpesが作り出したherpes骨感染症の結果に過ぎないのです。つまり38億年前に生命が生まれたのですがその後人類誕生の大昔から現在に至るまで癌という病気はなかったのです。直鎖ゲノムDNAを持ったヘルペスは4億年前にこの地球に生まれたのですがあらゆる生命は遺伝子を進化に進化を重ねて遺伝子を環境に合わせて突然変異させてあらゆる見えない病原体に打ち勝つ種を生み出して生き続けてきてたのです。
最高の進化の頂点に立っている人類が20万年前に誕生したときからさらに徐々に増えて行ったherpesウイルスは、従属栄養体ですから独立栄養体である多細胞生物に寄生するずるい策略を身につけたのですが多細胞生物も自分の身を微生物から守るための免疫系を進化させていきのびてきたのです。
先ず現代生物学における生物の定義とは何であり、更にヘルペスウイルスとは何でしょうか? 「生物の定義」は、(1)外界と膜で仕切られている、(2)代謝を行う、(3)自己複製する、3つの特性を持っています。ウイルスは、他の細胞に感染することで、自己複製を行うことによって生き延びてきたのです。ウイルスは、いくら栄養を与えても、単独で増殖することはありません。すべてのウイルスは、宿主となる細胞に感染しないと増殖できないのです。とりわけherpesウイルスは他のウイルスに比べようがないくらいに人間の最高に進化した免疫遺伝子から逃れるための進化を遂げたので人間の免疫では殺しきれない従って人間の免役にワクチンを作らせない進化を遂げ切ったのです。
Herpesウイルスの特徴は、①最小の微生物である(大部分は20~300nm)、ナノメータと読み10億分の1でherpesは平均200nmの大きさです。②細胞構造が無く、タンパク質と核酸からできている、③ウイルスの遺伝子を作る核酸の材料はDNAかRNAのいずれか一方を持つのですが、herpesウイルスはDNAです。④生きている細胞内でしか増殖できない偏性細胞寄生性です。⑤自分自身でエネルギーを産生せず、宿主細胞の作るエネルギーを利用する。⑥細胞内の増殖過程にはウイルス粒子が形成されていない「感染性が無い時期」があり、2分裂による増殖をしないことなどの6つが挙げられます。
偏性細胞寄生性(obligate intracellular parasitism)とは、特定の微生物が生きた宿主細胞の中でのみ増殖できる性質のことで、人工培地での増殖不可: これらの微生物は、通常の人工的な栄養培地では生育・増殖できません。宿主細胞への依存: 生きて機能している細胞の内部環境に完全に依存しており、宿主細胞が持つ代謝機能(特にATP合成など)を利用して、自身の増殖に必要なエネルギーや物質を獲得します。
偏性細胞寄生性を持つ主な生物には①ウイルス: 細胞構造を持たず、宿主細胞の複製機構を利用して増殖する、典型的な偏性細胞寄生体です。②細菌の一部のクラミジア属:DNA、RNA、リボソームを持ちタンパク質合成能力はありますが、ATPなどのエネルギー源を宿主細胞に依存しています。③リケッチア属:ダニやノミなどを介して感染し、細胞内でのみ増殖可能です。
偏性細胞寄生性とは生きた細胞内でしか増殖できないherpesウイルスのような微生物であり宿主の細胞を必要とし、その細胞の機能を利用して増殖するのです。ウイルスの細胞感染の目的は宿主細胞を利用した自己の複製と増殖にあります。
ウイルス粒子が形成されていない「感染性が無い時期」は、感染した宿主細胞の中に隠れています。この期間は「エクリプス期(eclipse phase)」と呼ばれ、ウイルスが宿主細胞に侵入してから、新しいウイルス粒子が細胞内で形成されるまでの期間を指します。
この「エクリプス期(eclipse phase)」の時期に感染性のあるウイルス粒子が検出されない理由はウイルスが感染活動を一時停止しているのではなく、新しいウイルス粒子を大量生産するための準備を、宿主細胞の内部で着々と進めている期間なのです。その順序は①ウイルスの分解: 宿主細胞に侵入したウイルスは、まず外殻(カプシド)が取り除かれ(脱殻)、内部の遺伝子(DNAやRNA)が露出します。この段階では、もはや完全なウイルス粒子として存在しません。②ウイルスの再プログラム: 露出したウイルスの遺伝子は、宿主細胞の複製・転写・翻訳のシステムを乗っ取ります。この期間、ウイルスは自らの遺伝子を複製し、新しいウイルス粒子を作るためのタンパク質を生産します。③部品の状態: 新しいウイルス粒子が完成するまでの間、ウイルスはバラバラの部品となっている遺伝子とタンパク質として細胞内に存在します。これらの部品は単体では感染性を持たないため、この段階では感染性は検出できません。④細胞内の閉じ込め: 感染性のある新しいウイルス粒子は、部品の組み立てが完了するまで宿主細胞内に留まっています。細胞外に放出されることで初めて、他の細胞を感染させることができます。ウイルス複製はウイルスの違いで大きく異なり、ウイルスに関与する遺伝子の種類に依存していますが、ほとんどのDNAウイルスは核内で集合するのに対し、ほとんどのRNAウイルスは細胞質内でウイルス複製が行われます。つまりヘルペスはDNAですから 核内で行われます。エクリプス期は特に、ウイルスの細胞内での増殖過程で、ウイルスが検出できなくなる期間を指す場合は日本語で「暗黒期(あんこくき)」と訳します。「暗黒期」に対して潜伏期とは感染した時点から症状が現れるまでの期間のことを指します。 潜伏期であっても感染性を有することが多くあります。さらに 感染性期とは、ヒトがヘルペスを他人に感染性を有する期間のことを指します。 潜伏感染期とは、感染した時点から感染性を有するまでの期間のことを指します。
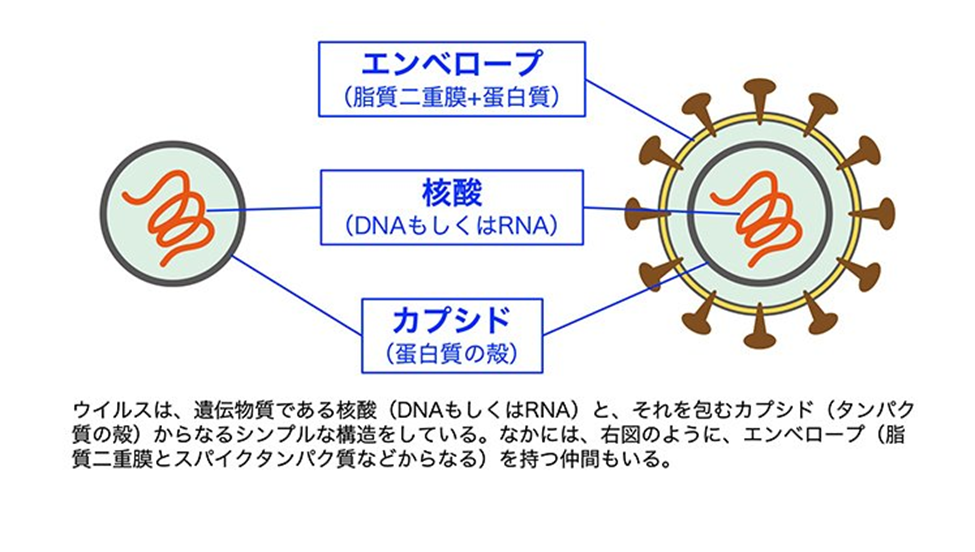
ウイルスの基本構造
ウイルスは、遺伝情報となる核酸とそれを囲むタンパク質(カプシド)が最小単位です。ウイルスの種類により、カプシドタンパク質の外側にエンベロープと呼ばれる脂質二重層の膜にherpesウイルスのようにスパイクタンパク質が刺さった膜を被っているものもあります。スパイクタンパク質はヘルペスが細胞に感染する際に使用されます。下の絵図はヘルペスウイルスで核酸はDNAです。す。
厚生労働がんに関する普及啓発懇談会で中川恵一先生が話された「がんに関する普及啓発」のための「癌の秘密」というタイトルの論文の間違いをサブタイトルごとに批判したいと思います。
まず「癌には秘密は何もありません」というのは癌という病気は存在しないから秘密があるはずもないのです。癌と言われる病気は正しくは「ヘルペス感染による増殖過剰細胞症」というべき感染症に過ぎないのです。しかし悲しいことにherpesは免疫で殺しきれないのでワクチンも作れないのです。何故ならばあらゆる細胞の核のゲノムに隠れてしまうから免疫はヘルペスを殺し切れないからです。ヘルペスは免疫が落ちた時と細胞が分裂するときにのみ子供のビリオンを大量に生み出し細胞の外に出て初めて免疫細胞に見つかります。
中川恵一
がんのひみつ「目次」「がん検診、ススメル理由」「自分で選ぶがん治療」「癌に負けない緩和ケア」がん検診も全く役に立たないのです。早期発見、早期治療をやっても癌細胞は存在しないので癌細胞と言われる細胞には増殖関連遺伝子を突然変異させたヘルペス感染細胞を早期発見してherpes満載の偽の癌細胞にいるherpes感染細胞を取り除き、更にherpesを放射線でかつ抗がん剤の三大医療で癌の原因であるヘルペスを殺すことができると思いますか?100%無理です。だからこそこの世にない癌患者が増え更にこの世にない癌死が増え続けているのです。
癌検診、癌治療、癌緩和ケア「癌検診、癌治療、癌緩和ケア」の3つとももすべて間違っているので最後は癌緩和ケアで安楽死させているだけなのです。
がんを知って、がんと向き合う癌を知ることは癌の原因はヘルペスで、がんと向き合うことは癌の原因となるherpesを自分で増やさないことであり免疫を抑える治療を受けないことです。
「目次」「がん検診、がん検診をススメル理由」「自分で選ぶがん治療」「癌に負けない緩和ケア」がん検診をススメル理由はすべて間違っています。自分で選ぶがん治療ほど無責任な選択はありません。癌について100%無知な患者に死に方を選択させるほど無責任な医療はありません。この選択は医者の責任放棄です。
「がん検診、ススメル理由」
がんがふえているのは日本の社会が癌を生み出すherpesが増え続けているからです。日本人が見かけは豊かな生活にもかかわらず免疫が落ちるストレスが増えかつ免疫を抑える医療が繁栄し続けているのでherpesが増えてしまったからです。
古いデータですが平成19年度の日本人の死亡は約110万人。令和4年の日本人の死亡は160万人です。このうち、がんによる死亡は約34万人ですので、日本人の3人に1人近くが、がんで亡くなっています。令和4年の日本人のがんによる死亡は約40万人です。毎年癌による死亡は増え続けています。65歳以上では、2人に1人が、がんで亡くなっています。
一方、日本人の2人に1人弱が、生涯にがんになると言われています。ますますがんは増えて行きます。何故ならばこれから先、全ての人のストレスは増大していき癌を含めてすべての病気の原因となるherpesもウナギ上りに増えて行きます。心の病はもとより先天性、後天性遺伝子病もすべての病気の原因となっている殺しきることができない増えるherpesがあらゆる細胞に感染して宿主のゲノムDNAにいとも簡単に入り込み宿主の遺伝子をherpesの遺伝子と入れ替えてしまい極めていとも簡単に突然変異させてしまい、その結果たまたま2種類の癌関連遺伝子(増殖関連遺伝子)に突然変異が起こってしまうと1個の癌細胞の誕生となるのです。勿論人の体には40兆個の細胞があるのでどこの組織の1個の細胞が癌細胞になったかは絶対に誰にもわかりません。10億個の癌細胞の塊が1センチの大きさで1グラムの重さになって初めて癌であることが発見されるのです。
1個の癌細胞がここまで大きくなるのに10年かかると癌の専門医はほざいていますがこれも嘘です。彼らの言い分は癌細胞は1年ごとに3回分裂するので10年たてば計算すれば10億個の癌細胞になると阿呆な間違った計算の結果を主張しているだけです。何故ならば1個の癌細胞がどれだけの速さで増えるかを決めるのはヘルペスウイルスが癌細胞どれだけのスピードで癌細胞や新しい正常な細胞に感染して2種類の癌関連遺伝子(増殖関連遺伝子)に突然変異を起こす速さによって決まる問題であるからです。免疫を落とし、更に幹細胞を持っている癌細胞や正常な細胞の増殖分裂する回数が増えれば増えるほど分裂した染色体に増えたヘルペスが姉妹染色分体のゲノムDNAにいとも簡単に入り込み、宿主の遺伝子をherpesの遺伝子と入れ替えてしまい、極めていとも簡単に突然変異させてしまい、その結果たまたま数百個もある2種類の癌関連遺伝子(増殖関連遺伝子)に突然変異が起こってしまう回数が増えるのでそれだけ癌化の度合いを増やしてしまう度合いが増えることになるからです。
つまりがんの進行度はヘルペスが増殖分裂して増えていくヘルペスの数が増える進行度によって決まるのです。現代の三大がん医療は要りようはすべて苦痛を伴う免疫を抑制をしてしまう間違った医療ですから癌を直すことは絶対に不可能なのです。ついでに付け加えると近頃高価な何の意味もない「免疫癌医療」が流行していますがすべてお金儲けのためだけに行われているのですべて癌を直すことができないのは何故でしょうか?その答えは極めて明快です。答は「癌細胞は自分自身の細胞が癌細胞(ヘルペスによって増殖過剰になった細胞)に過ぎないだけですから自己である細胞なのです。免疫の基本原理は「自己と非自己」とを100%見極めることからはじまるからです。この免疫の基本原理の「自己と非自己」を区別できなければ生命発生は38億年前ですがその長い長い進化の中で築き上げられた病原体から身を守るという免疫の世界は一挙に崩壊してしまい生命体は壊滅してしまうことになるでしょう。ところが医薬業界は一致協力して「自己免疫疾患」を作って病気を新たに捏造して病人を苦しめてお金を儲けて喜んでいるのです。この世界の中で最も恐ろしい怖がるべき世界が医薬業界なのです。自己免疫疾患も癌もこの世に存在しないので何も恐れることは無いのです。患者にとって最も恐ろしいのは医薬業界であり自己免疫疾患や癌を作った権威あるお偉い医学者であり製薬メーカーの指導的な薬学者たちなのです。
欧米では減っているがんの死亡者数が、日本では増えているのです。2人に1人が「がん」になり、3人に1人が「がん」で死ぬ。これは世界一の割合ですから、日本は「世界一のがん大国」と言えます。老人が増えたから「世界一のがん大国」になったのではなく間違った免疫を抑える医療システムが世界で最も充実しているのが日本であるからです。かつ日本は豊かそうですが実はストレスが多くても日本人は力を持っているお偉い人には黙って耐え続けすぎて知らぬ間に免疫を抑え続けすぎるのでこっそりヘルペスが増えていることに一般大衆は気が付いていないのです。
がん細胞とは
なぜ、日本は、「世界一のがん大国」になったのでしょうか?これに答えるには、がんという病気を知る必要があります。がんは、一言で言えば、「カラダの老化」と言えるのです。がんの原因は「カラダの老化」であるほど間違った説明はありません。その間違いの根拠を明らかにしましょう。「カラダの老化」つまり年老いた人の老化した細胞は実は癌と違って増殖しなくなるのです。何故でしょうか?本当は老化すればするほど癌細胞は増殖しなくなるのですが、一方、癌細胞は不死化して無限に増殖し続ける細胞なのになぜ人は老化してしまうと老化細胞は増殖しなくなるのでしょうか?
老化とは正常組織の細胞を培養すると、細胞分裂が約50回程度回数に達した時点でそれ以上分裂できなくなります。これをヘイフリックの限界と言います。これは分裂のたびに不可逆的な変化が積み重なるからであり、その変化というのはテロメア(teromere)の短縮です。23本の染色体の両末端部にあるテロメアには数ヌクレオチドのTTAGGGの反復配列があり、細胞が増殖・分裂するたびにヌクレオチドの6塩基のTTAGGGの反復配列(テロメア)が短くなっていくのです。しかしテロメアの部分に増殖・分裂の細胞周期の進行を制御するための遺伝子があるわけでもないのでテロメアが短くなるだけで突然に分裂が止まる理由がないのです。
実は「テロメアの短縮」そのものが細胞分裂が約50回程度回数に達した時点で細胞分裂をやめる直接の原因ではなく「テロメアの短縮」を異常事態として感知する細胞周期チェックポイントが働いたために細胞周期が分裂を止めてしまったためなのです。この細胞分裂を止めるために中心的な役割をするのは転写因子p53であるのです。だからこそ転写因子p53の働きを抑制するとテロメアが短くなっても細胞は更に分裂を続けるようになるのです。
細胞周期チェックポイントとは、細胞が細胞周期(細胞が増殖して分裂する過程)を正常かつ秩序正しく進んでいるかを監視し、異常がある場合は細胞周期の進行を一時的に停止させる制御機構です。この機構により、DNAの損傷や不完全な複製、染色体の不適切な配列といった異常が次の段階へ伝達されるのを防ぎ、正確な遺伝情報を次世代の細胞に伝える役割を果たします。
それでも最終的には染色体構造の維持そのものに支障をきたすような2本の染色体のテロメア同士が癒着をきたしてしまい、物理的に細胞分裂ができなくなってしまうのです。テロメアの短縮が本当の限界に達してしまうより前に分裂の停止という予防措置が取られるのです。
老化とは正常組織の細胞を培養すると、細胞分裂がある回数に達した時点で約50回程度分裂を繰り返すと、それ以上分裂できなくなります。これをヘイフリックの限界と言います。ヘイフリックの限界とは、アメリカの生物学者レナード・ヘイフリックが発見した、ヒトや動物の正常な細胞が持つ、分裂回数の自然な限界のことです。細胞分裂のたびに短くなる23本の染色体末端の「テロメア」が一定の長さになると、細胞は染色体(遺伝情報を持つDNA)を保護できなくなり、それ以上分裂できなくなり、細胞老化と呼ばれる状態に陥り、細胞老化により増殖を停止してさまざまな機能が変化していくのです。
ヘイフリックの限界の例外があります。がん細胞と幹細胞と生殖細胞にはヘイフリックの限界がないのです。何故でしょうか?さらに幹細胞やがん細胞や生殖細胞などの細胞にはテロメラーゼという酵素が存在し、テロメアの短縮を遅らせたり、テロメアを伸ばしたりするため、ヘイフリックの限界に縛られずに無限に分裂を繰り返すことができるのは何故でしょうか?
ヒトのテロメラーゼとは何でしょうか?染色体末端にある反復配列である6塩基(TTAGGG)でできたテロメアを伸長させる酵素です。細胞分裂のたびに短くなるテロメアの長さを維持し、細胞の老化を防ぐ役割を担いますが、正常な幹細胞(ES細胞、iPS細胞)と正常な生殖細胞など一部の細胞では活性化し、テロメラーゼは胎児が発達する間、細胞分裂が何度も行われて完全な体をつくるときに最も活発に働いています。 その後、ほとんどの細胞での活性はずっと下がり、テロメアは歳とともにだんだん短くなっていきます。因みにiPS細胞で作られた臓器の細胞が癌になるのは何故でしょうか?それはiPS細胞は人工多能性幹細胞であるからです。幹細胞とは皮膚や血液のように細胞の入れ替わりが激しい組織に存在する細胞です。失われた細胞を補充するための増殖・分裂を行う細胞のゲノムDNAにherpesのゲノムDNAを組み込み、増殖関連遺伝子を変異させて自分の子供であるビリオンを最大限増やすことができるのです。
テロメラーゼは、RNA鋳型と逆転写酵素の働きにより、染色体末端のテロメアに反復配列を付加します。これにより、テロメアの短縮を防ぎ、染色体の末端融合や構造の不安定化を防ぎます。徐々に老化して必要のない細胞の増殖・分裂が減っていくと正常な体細胞はテロメアが短くなると最後に分裂を停止(細胞老化)するのです。言い換えるとテロメラーゼは、細胞老化のためにあるのです。細胞老化は永遠に生きられない細胞にとっては必ず必要なのです。ところがherpesが感染した細胞は自分自身が増殖・分裂するために増殖関連遺伝子のみならず同時にテロメラーゼ遺伝子も変異させてしまいherpesがいつまでもテロメラーゼ遺伝子を変異させて活性化させて増殖過剰細胞(癌細胞)を人が死ぬまで、テロメアを維持し無限に分裂し続ける異常な細胞に仕立て上げてしまうのです。ヘルペスウイルスはなんて恐ろしいウイルスなのでしょうか!!!!
テロメラーゼが活性化している正常な細胞には細胞の増殖・分裂が必要な生殖細胞と幹細胞(ES細胞、iPS細胞)があります。最後は老化細胞になるためにテロメアが短くなり過ぎると細胞周期チェックポイントのp53の働きを介して細胞分裂を停止してしまい細胞は老化していくのです。
テロメアは遺伝情報を持っていない、DNA構造の集合体に過ぎないのです。このDNA構造の集合体を作るのがテロメラーゼであり、RNA鋳型と逆転写酵素の働きにより、染色体末端のテロメアに反復配列を付加されたのがDNA構造の集合体なのです。染色体の両側末端にあります。 染色体である遺伝子DNAがむき出しにならないように保護するキャップのような構造体です。テロメアは染色体の端にある保護キャップのようなもので、細胞が分裂するたびに短くなっていきます。ある程度短くなると細胞は分裂を停止し、これが細胞老化の原因の一つです。この短縮は「テロメアの時計」として機能し、異常な細胞の増殖を防ぐ役割も持ちます。しかし、一部の老化細胞はそのまま蓄積し、加齢に伴う様々な疾患の原因となることがあります。
テロメアはDNA構造の集合体であるにもかかわらず遺伝情報を持っていない染色体の一部であるDNAなのです。つまり遺伝子でないDNAなのです。DNAのすべてが遺伝子ではないのです。DNA全体の約1.5%の部分だけがタンパク質の設計図となる遺伝子に過ぎません。染色体はDNAという物質でできていますがテロメアのようにDNAでありながら情報を持たない例として、染色体のセントロメア(動原体)などがあります。セントロメアは染色体を形成・維持する構造であり、テロメアと同様に繰り返しの配列を持つことが多いですが、遺伝子としての機能は持ちません。
ヒトのDNAの大部分は「遺伝子」ではない部分であり、その量はDNA全体の約98.5%にも及びます。これらの遺伝子以外の部分は、遺伝子の働きを調節したり、DNAの構造を維持したりするなどの役割を担っていることが分かってきており、単に「ジャンク(がらくた)DNA」として無視されるべきものではなくなってきています。
ヒトDNAにおける遺伝子の割合
遺伝子の部分(タンパク質の設計図):DNA全体の約1.5%に過ぎません。
遺伝子でない部分:残りの約98.5%は遺伝情報を持たない部分で、遺伝子の働きを調節する役割を持つものや、その他多様な機能を持つ部分が含まれています。
遺伝子(タンパク質の設計図)以外のDNAの役割
遺伝子の調節機能:
DNAの多くの部分には、遺伝子がいつ、どこで、どれだけ発現するかを制御する機能があります。
構造的な役割:
DNAは染色体として細胞核に格納されており、その構造を維持するために、テロメアのような遺伝子以外のDNAが重要な役割を果たしています。
ヒトのDNAは、私たちが持つ個性や体を形作るタンパク質の設計図である「遺伝子」(1.5%)が大部分を占めるのではなく、遺伝子以外の部分(98.5%)が圧倒的に多いのが特徴です。これらの遺伝子以外のDNAは、遺伝子の機能を調節したり、ゲノムの構造を安定させたりする役割を担っており、生物の複雑な生命活動を支える上で不可欠な要素となっています。
細胞の老化を決定しているヘイフリックの限界は何が決めているのか?
細胞の老化を決定するヘイフリックの限界は、主に染色体末端の「テロメア」の短縮によって決まります。細胞分裂のたびにテロメアは短くなり、ある程度短くなると細胞はそれ以上分裂できなくなり、老化が始まります。テロメアは染色体を保護する役割を持ち、その長さが細胞の寿命時計のように機能しています。
テロメアと細胞分裂
細胞分裂とテロメアの短縮:細胞が分裂し、DNAが複製されるたびに、染色体の末端にあるテロメアの長さが短くなっていきます。
テロメアの役割:テロメアは、染色体の末端を保護するキャップのような役割を果たし、大切なDNAが失われるのを防ぎます。
老化の開始:テロメアが一定の短さに達すると、細胞はそれ以上分裂できなくなり、複製老化という細胞老化状態に入ります。
その他の要因
ストレス:酸化ストレス、放射線、がん遺伝子の異常活性化など、様々な外部からのストレスも細胞老化を誘導することがありますが、ストレスによって増えたヘルペスが人が死なない限りherpesは永遠に生き続け増大し続けるので酸化ストレス、放射線、がん遺伝子の異常活性化などは一過性のものですから、遺伝子を癌化させる度合いはヘルペスの無限大の影響と比較しようがありません。様々な外部からの強い長いストレスによる免疫抑制がherpesを増やし過ぎて癌になってしまうのです。くたばれherpesめ!!!!
防御機構:
細胞老化は、異常な細胞の増殖を抑え、がん化を防ぐ生体の防御機構の一つなのです。
複製老化という細胞老化状態になるメカニズムは何でしょうか?
複製老化は主にテロメアの短縮によって引き起こされる細胞の増殖限界です。細胞が分裂するたびに染色体の末端にあるテロメアが短くなり、テロメアが一定の短さに達すると、細胞分裂が妨げられDNA損傷応答が引き起こされることで、細胞は複製老化状態に入り増殖を停止します。
複製老化のメカニズム
テロメアの短縮:
染色体の両端にはテロメアと呼ばれる保護キャップのような構造があります。細胞が分裂するたびに、DNA複製時にテロメアは少しずつ短くなります。
ヘイフリック限界:
分裂を繰り返した結果、テロメアが非常に短くなり「限界長」に達すると、細胞はそれ以上分裂できなくなります。この細胞が分裂できる回数に限界がある現象をヘイフリック限界といいます。
細胞老化の誘導:
短くなったテロメアはDNA損傷とみなされ、DNA損傷応答が開始されます。これにより、細胞周期の停止(細胞老化)が誘導され、細胞は分裂を止めるのです。
複製老化とがん化の関係とテロメアがさらに短くなると「クライシス」と呼ばれる状態に陥り、染色体の不安定化と変異の蓄積が進むのは何故か?
複製老化は、無制限に分裂し続けるがん細胞の増殖を抑制する役割があります。
複製老化を抑制すると細胞は増殖を続けますが、この段階でテロメアがさらに短くなると「クライシス」と呼ばれる状態に陥り、染色体の不安定化と変異の蓄積が進みます。
このクライシスを乗り越えたごく一部の細胞が、無限増殖能力を獲得し、がん化するのは癌細胞を生み出したherpesウイルスが正常に発現していないテロメラーゼの遺伝子を突然変異を起こしテロメラーゼの遺伝子をも同時に変異させたためです。
テロメラーゼ遺伝子とは一体何でしょうか?
テロメラーゼ遺伝子(TERT遺伝子)は、染色体の末端にある蛋白の集合体であるテロメアを長くする酵素「テロメラーゼ」のタンパク質部分(テロメラーゼ逆転写酵素:hTERT)を作るための設計図となる遺伝子です。TERT遺伝子は、テロメラーゼ逆転写酵素の英語表現「telomerase reverse transcriptase」の略称であり、テロメアを伸長するテロメラーゼの触媒サブユニットをコードしています。特に、ヒトのTERT遺伝子は「hTERT」と略されることがあります。
hTERTは、「human telomerase reverse transcriptase」の略称であり、テロメラーゼの逆転写酵素サブユニットを指します。テロメラーゼは染色体末端のテロメアの伸長を担う酵素で、hTERTはその主要な構成要素であり、テロメアにTTAGGGという配列を付加する機能を持っています。
hTERTの主な役割
テロメア伸長:
染色体の末端にあるテロメアが短くなるのを防ぎ、細胞の増殖に必要なテロメアの長さを維持します。
この遺伝子は全ての正常な細胞に存在しますが、生殖細胞や幹細胞以外の多くの体細胞では機能が必要ではないので抑制されており、テロメラーゼの活性が低い状態にあります。テロメラーゼは、細胞分裂のたびに短くなるテロメアを伸ばすことで、細胞老化を抑制し、最後に細胞の老化が必要になるとテロメラーゼの活性がなくなります。
テロメラーゼ遺伝子の役割
テロメラーゼ酵素の生成:
TERT遺伝子はヒトテロメラーゼ逆転写酵素(human telomerase reverse transcriptase略hTERT)をコードしており、この酵素はテロメアの伸長に不可欠です。
細胞の不死化:
テロメラーゼ活性を持つ細胞(生殖細胞、幹細胞、がん細胞)は、テロメアの短縮を回避し、無限に増殖する能力を持つことができます。
テロメラーゼ遺伝子と細胞の状態
体細胞のテロメラーゼ:
通常の体細胞ではテロメラーゼの働きは抑制されており、テロメアが短くなることで細胞分裂の回数が制限され、細胞老化が起こります。
がん細胞のテロメラーゼ:
多くのがん細胞では、TERT遺伝子の発現が上昇してテロメラーゼが活性化し、テロメアを維持することで無限増殖を可能にしています。
再生医療におけるテロメラーゼ:
iPS細胞やES細胞のような幹細胞はテロメラーゼ活性を持つため、半永久的な分裂が可能であり、テロメラーゼは再生医療にも関連しています。
テロメラーゼ遺伝子と疾患
先天性角化異常症:
テロメラーゼの機能不全が原因で発症する疾患で、患者のテロメア長が著しく短いことが特徴です。胎児の時に母親がヘルペスにかかってテロメラーゼの遺伝子を突然変異させてしまい正常なテロメラーゼ酵素蛋白が発現できなくなりテロメラーゼの機能不全が原因で発症したのです。先天性角化異常症の多くは、遺伝子の変異が原因で発症する先天性の遺伝子病です。具体的には、テロメアという染色体の末端部分に関わる遺伝子の異常がヘルペスの遺伝子組み換えによって引き起こされることが多く、皮膚のバリア機能が十分に働かないことが病気の背景にあります。
遺伝性について
遺伝子の変異が原因:
多くの場合、生まれつきの遺伝子の変異が原因で発症します。
テロメアの異常:
特に「先天性角化不全症」などの一部の先天性角化異常症では、染色体の末端にあるテロメアの維持や修復に関わる遺伝子の異常が原因となります。
先天性の要素
生まれつきの疾患:
遺伝子の変異が原因であるため、生まれつき発症する病気です。
早期の診断:
多くの場合、幼少期から症状に気づき、診断されることが多いです。
がん治療:
テロメラーゼ阻害剤は、がん細胞の増殖を抑制する新たながん治療薬として期待されていますが根本の原因はヘルペスですから、テロメラーゼ阻害剤は対症療法ですから無意味です。アッハッハ!!!
TERT遺伝子はヒトテロメラーゼ逆転写酵素(human telomerase reverse transcriptase略hTERT)をコードしており、何故この酵素はテロメアの伸長に不可欠なのか?
ヒトテロメラーゼ逆転写酵素(hTERT)は、テロメラーゼ複合体の主要な部分であり、RNA鋳型(TER)を使い、染色体の末端にあるテロメアに「TTAGGG」という繰り返しDNA配列を付加する逆転写酵素活性を持っています。この酵素は、細胞分裂の度に短くなるテロメアを伸ばし、細胞の不死化や寿命維持に寄与しますが、herpesによって生まれたがん細胞で活性が上昇し無限に分裂する性質(不死化)に関わることが知られています。
テロメラーゼのメカニズム
1. RNA鋳型の利用:
テロメラーゼは、RNA構成要素(TER)を鋳型として持っています。このRNAには、ヒトのテロメア配列である「TTAGGG」のコピーが含まれています。
2. テロメアへの結合:
テロメラーゼ複合体は、既存のテロメア配列のG連続部分を認識し、その部分に結合します。
3. 逆転写によるDNA合成:
hTERTは、自身のRNA鋳型を読み取り、DNA塩基をDNA鎖に結合させる逆転写反応を行います。これにより、「TTAGGG」の繰り返し配列をテロメアの末端に伸長させます。
4. テロメアの維持:
このプロセスを繰り返すことで、細胞分裂の度に短くなるテロメアの長さを維持し、細胞が正常な分裂を継続できるようにします。
テロメラーゼの役割
細胞の不死化:
幹細胞や生殖細胞、そしてがん細胞では、テロメラーゼの活性が維持されます。これにより、テロメアが短くなるのを防ぎ、これらの細胞が分裂を繰り返すことができます。
がんの発生と進行:
多くのがん細胞ではテロメラーゼが過剰に発現しており、テロメアを無限に伸長させて自己の永続的な増殖を可能にしています。
このように、ヒトテロメラーゼ逆転写酵素は、テロメアを伸長させる「テロメア維持酵素」として、細胞の分裂と生命維持に不可欠な役割を果たしています。
TERT遺伝子がコードするヒトテロメラーゼ逆転写酵素(hTERT)は、テロメアの末端に繰り返し配列(TTAGGG)を付加することでテロメアを伸長させる機能を持つため、テロメアの伸長に不可欠です。テロメラーゼは、染色体の末端を保護し、正常な細胞の分裂によるテロメアの短縮を防ぎ、細胞の老化を遅らせる働きがあります。
hTERTの主な役割
テロメアの伸長:
TERT遺伝子によってコードされるhTERTは、テロメラーゼの触媒サブユニットとして機能し、RNAテンプレートを使い逆転写反応によってテロメアの末端にTTAGGGという繰り返し配列を付加します。
ゲノムの安定性維持:
テロメアが伸長されることで、染色体の末端が保護され、細胞分裂のたびに起こるDNAの損傷を防ぎ、ゲノムの安定性を維持します。
細胞の不死化:
正常な体細胞ではhTERTの発現は低いかありませんが、がん細胞ではhTERTの発現が亢進され、テロメアの維持が可能になるため、がん細胞の無限増殖と不死化につながります。
hTERTが不可欠な理由
細胞が分裂するたびに、染色体の末端にあるテロメアは短くなります。テロメアが極端に短くなると、細胞分裂が停止し、細胞老化を引き起こします。hTERTは、このテロメアの短縮を補う「テロメラーゼ」という酵素の重要な構成要素であり、テロメアを伸長させる唯一のメカニズムです。そのため、細胞が世代を超えて分裂を続けるためには、hTERTの活性が不可欠なのです。
「寿命時計」とは何でしょうか?
テロメアの長さが細胞の分裂回数を制限して長生きしすぎて、老化し過ぎないようにしてくれているのです。つまりテロメアの長さは寿命の長さとなるのでテロメアを「寿命時計」と言います。
テロメラーゼはすべての細胞が持っているわけではなく、生殖細胞、幹細胞、がん細胞といった特定の細胞に限り活性化しています。通常の体細胞ではテロメラーゼの活性が抑えられているため、分裂を繰り返すうちにテロメアが短縮し、細胞は老化(細胞分裂の限界)を迎えます。
テロメラーゼが活性化する細胞の例
生殖細胞:
次世代に遺伝情報を伝える役割を持つ細胞で、テロメアの長さを一定に保つためにテロメラーゼが常に機能しています。
幹細胞:
細胞の供給源として、新陳代謝で失われた細胞を補うために分裂を繰り返します。テロメラーゼの活性により、長期にわたる分裂が可能になっています。因みに幹細胞を持っている細胞だけにヘルペスは感染して癌を作ることができるのです。
がん細胞:
ヘルペスによるテロメラーゼの異常な活性化によりテロメアの短縮が防がれ、無限に分裂し続けることで「不死化」します。
テロメラーゼが活性化しない細胞の例
通常の体細胞:テロメラーゼの活性が低く抑えられているため、分裂を繰り返すとテロメアが短くなり、最終的に細胞は分裂しなくなります。
このように、テロメラーゼの有無や活性の度合いは細胞の機能や運命を大きく左右します。
テロメラーゼの遺伝子を持っている細胞は限られているのですか?
はい、テロメラーゼはすべての細胞が持っているわけではなく、正常な細胞では生殖細胞、幹細胞、異常になった細胞ではがん細胞といった特定の細胞に限り活性化しています。通常の正常な体細胞ではテロメラーゼの活性が抑えられているため、分裂を繰り返すうちにテロメアが短縮し、細胞は老化(細胞分裂の限界)を迎えます。
テロメラーゼが活性化する細胞の例
生殖細胞:
次世代に遺伝情報を伝える役割を持つ細胞で、テロメアの長さを一定に保つためにテロメラーゼが常に機能しています。
幹細胞:
細胞の供給源として、新陳代謝で失われた細胞を補うために分裂を繰り返します。テロメラーゼの活性により、長期にわたる分裂が可能になっています。
Herpesが作ったがん細胞:
テロメラーゼの異常な活性化によりテロメアの短縮が防がれ、無限に分裂し続けることで「不死化」します。
テロメラーゼが活性化しない細胞の例
通常の体細胞:テロメラーゼの活性が低く抑えられているため、分裂を繰り返すとテロメアが短くなり、最終的に細胞は分裂しなくなる細胞分裂の限界を迎えます。
テロメラーゼの本来の働きと遺伝子
テロメラーゼの日本語の呼び方は、カタカナで「テロメラーゼ」と表記されるほか、その機能を示す「テロメア伸長酵素」、または「テロメア伸長酵素逆転写酵素」とも呼ばれます。これらはすべて、染色体の末端にあるテロメアを長くする酵素を指す言葉です。テロメラーゼは、染色体の末端にある「テロメア」という保護構造を伸長する酵素で、本来の働きは細胞分裂を繰り返す生殖細胞や幹細胞のテロメアを維持し、寿命を保つことです。テロメラーゼの設計図となる遺伝子(hTERT遺伝子など)は全ての細胞に存在しますが、多くの体細胞ではテロメラーゼは発現が抑制されており、テロメアは細胞分裂のたびに短くなり細胞老化を促します。
テロメラーゼの本来の働き
テロメアの伸長:
テロメラーゼは、逆転写酵素として機能し、細胞分裂のたびに短くなるテロメアのDNA配列を補充して、テロメアの長さを維持します。
生殖細胞や幹細胞の維持:
精子や卵子を作る生殖細胞、および幹細胞ではテロメラーゼが活発に働き、細胞が無限に増殖できるようにします。これにより、子孫の寿命や組織の維持が可能になります。
細胞老化の防止:
テロメラーゼがテロメアを保護することで、細胞の寿命を延ばし、個体の老化を遅らせる役割があります。
テロメラーゼの遺伝子
テロメラーゼの設計図は各細胞に存在する:
テロメラーゼを構成するタンパク質を作るための遺伝情報(遺伝子)は、人の体全体の全ての細胞に存在しています。
遺伝子の発現調節:
しかし、多くの体細胞ではテロメラーゼの遺伝子が「オフ」になっているため、テロメラーゼが作られず、テロメアは短くなります。多くの場合、体細胞のテロメラーゼ遺伝子は増殖・分裂しないときだけオフになるのではなく、もともと発現が抑制されているか、非常に弱い活性しか持っていません。テロメラーゼはテロメアの伸長に関わる酵素であり、体細胞が無限に分裂することなく寿命を迎え、異常な増殖を防ぐ役割があるため、発現が低い状態に保たれています。
体細胞におけるテロメラーゼの働き
本来の機能:
テロメラーゼは、細胞が分裂を繰り返すたびに短くなるテロメアを伸ばし、染色体の末端を保護する酵素です。
体細胞の抑制:
ほとんどの体細胞では、テロメラーゼの遺伝子の発現が厳密に制御されており、テロメアの長さが細胞の分裂回数を制限する「寿命時計」として機能します。
過剰な分裂の防止:
もし体細胞でテロメラーゼが活性化すると、テロメアが無限に伸び続け、細胞が無制限に分裂するようになります。これはがん細胞の特性であり、テロメラーゼの活動が細胞の異常な増殖や老化を防ぐ上で重要な役割を果たしていることがわかります。
対照的な細胞での例
生殖細胞や幹細胞:生殖細胞や幹細胞、そしてherpesによって異常な細胞にされてしまったがん細胞ではテロメラーゼの活性が高いことが知られています。これは、これら特定の生殖細胞や幹細胞が無限に分裂し続ける必要があるためですが、herpesによって異常な細胞にされてしまったがん細胞ではherpesによってテロメラーゼの活性が異常に高められてしまったからです。
がん細胞との関連:
ヘルペス感染によるがん細胞(増殖過剰細胞)では、テロメラーゼの遺伝子が異常に活性化(オン)されることが多く、その結果、テロメアが無限に維持されて細胞が無尽蔵に増殖する「不死化」が起こります。
テロメラーゼは癌化を防ぐために細胞老化によって発現しなくなるのですがそのメカニズムは何か?
テロメラーゼは、ほとんどの体細胞では細胞老化によって発現が抑制され、テロメアの短縮を促すことで、細胞が無限に分裂増殖する「不死化」を防ぎ、癌化を抑制します。細胞が分裂するたびに染色体の末端にあるテロメアは短くなりますが、テロメラーゼが発現しないことで、テロメアが短くなりすぎると細胞は分裂を停止し、老化して癌化を防ぐという仕組みです。
テロメラーゼの役割と細胞老化の関係
テロメアの短縮と複製老化:
細胞が分裂を繰り返すと、DNAの末端にあるテロメアが短くなります。テロメアが一定の長さまで短くなると、細胞は分裂を停止して老化し、この現象を複製老化(ヘイフリック限界)といいます。
テロメラーゼの不活性化:
ほとんどの体細胞では、細胞老化によってテロメラーゼの遺伝子発現が抑制され、テロメラーゼが働かなくなります。これによりテロメアがさらに短縮され、細胞の増殖が停止します。
癌化の抑制:
テロメアの短縮によって細胞の分裂能力が制限されることが、癌化を防ぐための重要なメカニズムです。癌細胞ではテロメラーゼが再活性化し、テロメアを延長させることで無限に分裂増殖する能力(不死化)を獲得して癌化に至りますが、通常の体細胞ではその抑制が働くため、不死化が阻まれ癌化が防がれます。
まとめ
テロメラーゼの発現抑制は、細胞が老化によってテロメアを短くし、細胞が不必要に増殖し続けることを防ぐメカニズムであり、細胞の不死化とそれに伴う癌化を抑制するために不可欠な役割を果たしています。
正常な細胞が癌になるのはヘルペスが感染できる増殖可能な幹細胞と生殖細胞だけであるのは何故でしょうか?何故ならば、あらゆる細胞の中でヘルペスが癌を作るためには感染した細胞のゲノムDNAに侵入しなければ細胞のがん関連遺伝子である増殖関連遺伝子に入りこんでこれらの遺伝子を突然変異させなければならないからです。従ってherpesが癌化できる細胞は増殖・分裂できる幹細胞と生殖細胞だけに限られるからです。難解ですがもっと詳しく説明しましょう。
herpesウイルスが細胞の遺伝子を癌化するためには細胞が増殖・分裂できる幹細胞と生殖細胞の染色体に感染できるのは細胞が増殖(2倍)するときに46本の相同染色体が2倍の姉妹染色分体がバラバラになった隙間だらけの姉妹染色分体に分かれた92本になるときにしかチャンスがないからです。何故ならば増殖する直前の凝縮した父と母からもらった対になった23本の頑丈な構造をした染色体のDNAには絶対に入り込めないからです。染色体のDNAがばらばらになって初めてherpesウイルスは染色体に感染可能であることを更に詳しく説明しましょう。
遺伝子(DNA)の運び屋であるDNAの二重螺旋構造体に囲まれた染色体の頑丈な構造の成り立ちについて。ヘルペスウイルスが簡単にDNAの二重螺旋構造の中にある染色体のゲノムDNAに入り込めないのは何故か?DNAの立体構造の二重螺旋構造や染色体とは何か?
染色体は細胞の核内に存在する、DNAとタンパク質が折りたたまれた構造体で、遺伝情報を担います。DNAという遺伝情報を収めた細長いひも状の分子が、ヒストンというタンパク質に巻きつくことでコンパクトに折りたたまれ、染色体となります。生物によって染色体の数は異なりますが、ヒトでは合計46本(23対)あり、この中に数百から数千個の遺伝子が配列しています。
染色体の構造と役割
1、DNAとタンパク質の複合体:
DNAは非常に長い分子であり、そのままでは細胞の核におさまらないため、ヒストンと呼ばれるタンパク質に巻きつき、コイル状に折りたたまれることでコンパクトな形になります。
2、遺伝子の運び屋:
染色体には多数の遺伝子が含まれており、生物の体や蛋白質を作るための設計図となる遺伝情報を親から子へと伝達する役割を担っています。遺伝物質であるDNAは細胞の中では染色体という形で存在しており遺伝子は染色体の上に決まった順序で並んでいます。ひとの場合46本の染色体に23500個の遺伝子が振り分けられています。染色体1本あたりの遺伝子の数は約500個~2800個が並んでいます。
3、細胞分裂のサポート:
細胞が分裂する際には、染色体は複製され、正確な数の染色体が二つの細胞に分配されます。このとき、染色体はさらに凝縮し、顕微鏡で観察できる棒状の形になります。
ヒトの染色体
ヒトの細胞には、常染色体22対(計44本)と性染色体1対(計2本)の、合計46本の染色体があります。
常染色体は1番から22番まで番号が付けられており、性染色体にはX染色体とY染色体があります。男性は「XY」、女性は「XX」の組み合わせを持っています。
なぜ「染色体(chromosome)と呼ぶのか?
「染色体(chromosome)」という名前は、細胞分裂中に特定の色素でよく染まる(染色される)ことから名付けられました。細胞分裂中に染色体を観察する際には、塩基性色素である酢酸カーミン溶液や酢酸オルセイン溶液で染色すると、細胞核中の染色体が赤く染まり、顕微鏡で観察しやすくなります。これらはDNA(負に荷電)と結合しやすい性質を持つため、核内の染色体を効率的に可視化できるのです。
染色体はDNAがヒストンと呼ばれるタンパク質に巻きつき、さらに数珠状に連なった「ヌクレオソーム」という構造を経て、非常に高密度に折りたたまれた頑丈な構造をしています。また、染色体の末端はテロメアによって保護されており、中央部には染色体を二つに分けるためのセントロメアといった、特定の機能を持つ構造も存在します。
染色体(クロモソーム)の頑丈さを支える構造は①ヒストンと②ヌクレオソームと③クロマチン(染色質)と④クロモソーム(染色体)と⑤DNAの二重螺旋構造の5つから成り立っている。
遺伝情報を担うDNAは、①ヒストンと呼ばれるタンパク質に約2回巻きつき、糸巻きのような「ヌクレオソーム」を形成します。②ヌクレオソームとは、真核生物の細胞核内でDNAが「ヒストン」と呼ばれるタンパク質に巻き付いて形成される、DNAの「基本単位」です。この構造は、ヒストン八量体という8つのヒストンタンパク質の中心にDNAが約1.75回巻き付いた形をしており、DNAをコンパクトに収納すると同時に、必要な時にDNAの情報を読み出せるようにする役割があります。複数のヌクレオソームが連なることで③「クロマチン」という長い繊維状の構造が作られ、さらに折り畳まれて④染色体(クロモソーム)となります。最後はDNAの二重螺旋構造となります。
ヌクレオソームとクロマチンの違いはヒストンとDNAが結合した構造を、ヌクレオソームといいます。 ヌクレオソームは、1個ヒストン+DNAの1セットをいいます。 ヒストン+DNAが結合して連なる構造をヌクレオソームと言いヌクレオソームが集まった状態を、クロマチンといいます。
ヌクレオソームの連鎖:
形成されたヌクレオソームが数珠のように連なることで、DNAは非常にコンパクトに折りたたまれ、細胞核内に効率的に収納されます。
テロメアによる保護:
染色体の末端にはテロメアと呼ばれる特殊な構造があり、DNAがむき出しになって損傷したり、細胞分裂の際に情報が失われたりするのを防ぎます。
セントロメアの機能:
染色体の中央部にはセントロメア領域があり、細胞分裂の際に紡錘糸が結合して染色体を均等に分配する役割を担います。
これらの構造が複合的に作用することで、細胞分裂の際に必要な遺伝情報を保持しながら、DNAを細胞核内に安定して収納できる頑丈な構造が維持されています。このような頑丈な遺伝子DNAの二重螺旋構造体に囲まれた染色体の頑丈な囲みを破って、ヘルペスは細胞のゲノムDNAに潜り込むために細胞分裂のときに染色体がバラバラになった92本の姉妹染色分隊の1本、1本を利用するので、自由自在にバラバラの92本の好きな1本の長い染色体(DNA)にヘルペス自身の短小なばらけた2本の染色体(DNA)の1本を簡単に組み入れることができるのです。
テロメラーゼが突然変異して起こる癌とはどのようにして生まれるのか?
テロメラーゼの「突然変異」というよりは、通常は活性を抑えられているテロメラーゼが、herpesによる発がん過程で異常に活性化する(悪性化・不死化)ことが、がん細胞の性質として知られています。herpesによって異常にされたテロメラーゼ再活性化は染色体の末端であるテロメアを伸長させることで、細胞の寿命を延ばし、無限に分裂できる「不老不死」の性質をがん細胞に与える酵素なのです。しかし癌細胞も最後はヘルペスの無限大に増えすぎた子供であるヘルペスビリオンにエネルギーや5大栄養素も何もかも奪われてしまい「不老不死」の酵素である蛋白酵素であるテロメラーゼも作れなくなって癌細胞も生きられなくなりヘルペスウイルスと一緒に死に絶えるのです。
テロメラーゼとがんの関連性
細胞の不死化:
正常な細胞はテロメアが短くなるにつれて老化し、分裂できなくなりますが、がん細胞ではテロメラーゼが活性化することでテロメアが維持され、細胞は無限に増殖します。
ほとんどのがんで活性化:
多くのがん細胞でテロメラーゼが発現していることが観察されており、がんの発生や進行に深く関わっています。
発がん過程での「悪用」:
元々、テロメラーゼは幹細胞や生殖細胞などでテロメアを長く保ち幹細胞や生殖細胞が増殖・分裂のために働く酵素ですが、herpesによって突然変異されて異常な癌細胞(増殖過剰細胞)になってしまいさらにテロメラーゼという酵素も再活性させられてテロメアも増え続けるだけの話に過ぎないのです。
癌細胞とは正常な細胞の2種類の増殖関連遺伝子がヘルペス感染細胞のゲノムDNAに組み込まれたヘルペス自身のゲノムDNAと入れ替わってしまい、この時に2種類の増殖関連遺伝子が遺伝子組み換えによる突然変異によって異常になってしまう細胞に過ぎないのです。正常な増殖関連遺伝子の2種類が突然変異したのは確かなのですがこの増殖関連遺伝子の総数は100個から数百個あるので特定の増殖関連遺伝子を挙げることはきわめて無理ではないのですが人の手と時間とお金と装置がいるので難しいのです。
本来増殖を正常に制御する遺伝子は複数あり、癌になる前の正常な遺伝子を増殖遺伝子と言います。突然変異して癌遺伝子になるのでこの増殖遺伝子をオンコジーン(がん原遺伝子)と言います。ところが正常な増殖過剰にならせない遺伝子を増殖抑制遺伝子というのですがこれもヘルペスのために突然変異して癌遺伝子になるので腫瘍抑制遺伝子とも言われるのです。オンコジーン(がん原遺伝子)は細胞の増殖を促進するのですが、腫瘍抑制遺伝子は増殖を抑制する役割を担っており、これらの2種類の遺伝子がヘルペスで突然変異させられると1個の癌細胞の誕生となるのです。この世には癌という特別な病気は存在しないので癌細胞という名前は止めて単純に増殖過剰細胞という正しい病名に変えるべきです。もちろん癌細胞と言う名前は医者が勝手に捏造しただけですから正しくは増殖過剰細胞(癌細胞)と言い換えて癌という死と結びつく最悪のイメージを連想させる名称は即廃止すべきなのです。老人性痴呆を認知症と言い換えたように変えるべきなのです。
この増殖関連遺伝子の総数は100個から数百個あるので数多くの増殖関連遺伝子がヘルペスのためにいわゆる癌化してしまえばこの癌細胞の悪性度や進行度や分裂速度のみならず癌の原因となるherpes自身の増殖分裂速度も増えその細胞を殺してしまういわゆる溶解感染となるのです。殺した細胞から生まれた膨大な数のビリオンが放出され次々とヘルペス感染細胞も新たに増えビリオンherpesは新たな癌細胞を作り出していくのです。
がんの転移というのは正しくはヘルペスが感染細胞を増やすことで新たなる癌細胞を生み出しているだけで癌細胞が別の組織に転移するメカニズムについては誰も明確にしておりませんのでそれまでは転移癌はヘルペス転移細胞と仮につけておきます。従ってがんの転移はヘルペスの感染による新しい組織の細胞に感染して生まれた新たなる原発性のヘルペス性癌細胞の誕生と考えるべきなのです。つまりこの世に転移癌もないのです。そのうち原発性の癌細胞が原発癌から離脱してリンパ管や血管に入り込んで新たなる組織に入り込み新たなる原発性の細胞がんが生まれるメカニズムが明らかになるまでは転移癌ではなくherpes感染症による新たな癌であるに過ぎないと考え続けることになるでしょう。ワッハッハ!!!!だれか正しい答えを教えてください。
オンコジーン(がん原遺伝子)別名、増殖遺伝子とは細胞の増殖や分化を促進する働きを持つ正常な遺伝子です。この遺伝子にherpesによる突然変異が起こると、細胞の増殖が過剰になり、がんを引き起こすのです。
腫瘍抑制遺伝子(別名、増殖抑制遺伝子細胞):細胞の過剰性増殖を抑制したり、細胞の異常な増殖を抑えたりする働きを持つ遺伝子です。ヘルペスが変異を起こすとこの遺伝子が機能しなくなり、細胞の増殖が制御されずに過剰になり、がんの原因の一つとなるのです。オンコジーン(がん原遺伝子)別名、増殖遺伝子と腫瘍抑制遺伝子(別名、増殖抑制遺伝子)の2種類の遺伝子がヘルペスによって突然変異させられると1個の癌細胞の誕生となるのです。
増殖関連遺伝子(癌関連遺伝子)とがんの関係
正常な細胞は必要に応じて増殖・分裂しますが増殖・分裂が終われば、必要なくなり増殖を停止します。
オンコジーン(がん原遺伝子)と腫瘍抑制遺伝子の両方正常であれば、この正常な細胞の増殖を適切にコントロールできているのです。ところがこれらの二つの遺伝子のどちらか一つがヘルペスによって突然変異させられると良性腫瘍が生まれますが悪性腫瘍ではありません。両方に突然変異の異常が生じると、細胞は制御されないまま増殖し、1個の癌細胞である悪性腫瘍が生まれ最終的には目に見えるがん細胞となる可能性があります。しかし免疫を回復させてherpesがその後新たに増えない限りはつまりヘルペスが再活性しない限りは細胞の増殖・分裂があっても癌細胞に潜伏感染しているherpesの増殖もなくなり、増えたヘルペスが新たなる新しい細胞に感染していく心配は必要ないので新しい癌細胞も増えることは無いのです。
とにかくherpesを増やさないようにストレスをかけない心掛けが何よりも大切です。それ以上に大事なことは病気で医者にかかっても免疫を抑制する対症治療は絶対にしないことです。この原則を一生守れば新たなる100個から数百個ある増殖関連遺伝子の突然変異が起こらないので癌細胞は増えることはないのです。言い換えるとすべてに人はヘルペスに感染していますから40兆個の細胞の内、すでに何個かの癌細胞(増殖過剰細胞)を持っている人も必ずいるはずですがherpesウイルスが増えない限り、言い換えるとストレスを避けて免疫を落とさない限りヘルペスを潜伏感染をさせ続けヘルペスを細胞内で増やさない限り癌は絶対に起こらないと断言できます。その自信のないヒトは私の様に抗ヘルペス剤を大量投与してヘルペスの増殖を予防できるのです。がん予防投与している人は私の患者さんにも何人かすでにおられます。抗ヘルペス剤は癌を直せる原因療法でもあるのは当然ですが抗ヘルペス剤は癌を予防できる最高の原因を増やさない根本がん予防薬となるのです。癌になりたくない人にお勧めします。
人の幹細胞を持っている細胞の総数はいくつか?人の体に含まれる幹細胞の正確な総数は不明ですが、成人では新生児期に比べて減少し、60歳で約1.5億個まで減少することがわかっています。体全体には約37兆個の細胞が存在し、幹細胞はそれらの中で自己を複製し、他の様々な細胞に分化する能力を持つ特別な細胞です。
幹細胞の数と減少
新生児期:新生児には約1.9億個の幹細胞が存在します。
加齢による減少:年齢とともに幹細胞の数は減少し、20歳では約10億個、60歳では約1.5億個まで減少します。これは、細胞分裂を繰り返すことによる劣化や、細胞分裂の制約が原因と考えられています。
幹細胞の役割
細胞の補充と組織の修復:
幹細胞は、病気や怪我によって失われた細胞を補充し、傷ついた組織を修復・作り替える役割を担っています。
恒常性の維持:
自己複製能力と多分化能力により、新しい細胞を生み出し、体の恒常性を保つ働きをします。
全体的な細胞数
成人には約37兆個の細胞があると言われており、その中の一部の細胞が幹細胞です。
幹細胞は全身に分布しており、傷ついた部位からのシグナルを受けてそこに集まり、組織の機能回復に貢献します。
正常なテロメラーゼは、細胞分裂のたびに短くなる染色体末端のテロメアを、[TTAGGG]の繰り返し配列を伸長させることで維持し、細胞の老化や死を防ぐ酵素です。主に生殖細胞や幹細胞に存在し、細胞の増殖能力を長期にわたって維持する役割を担っています。この働きにより、細胞は複製老化を回避し、組織の健康と機能の維持に貢献します。
テロメラーゼの主な働き
テロメアの伸長:
テロメラーゼは、リボ核タンパク質であり、テロメアの末端に6塩基からなる反復配列([TTAGGG])を追加してテロメアを長くします。リボ核タンパク質(RNP)とは、リボ核酸(RNA)とタンパク質の複合体の総称です。タンパク質合成の場であるリボソームや、核内でmRNA前駆体の成熟に関わるスプライソソームなどがあります。
リボ核タンパク質の主な役割とは
タンパク質合成:リボソームはRNAとタンパク質からなる複合体で、mRNAの遺伝情報に従ってアミノ酸を結合させタンパク質を作り出します。
転写後調節:核内低分子リボ核タンパク質(snRNP)などのRNPは、mRNA前駆体の成熟プロセスであるスプライシングに関わります。
転写後調節の制御:RNA結合タンパク質(hnRNPなど)は、mRNAの安定化、局在、成熟など、mRNAが核から核外へ輸送される過程において重要な役割を果たします。
ウイルス機能:インフルエンザウイルスの複製では、ウイルスゲノムRNAとタンパク質が結合したRNPが中心的な役割を担っています。
リボ核タンパク質の構造と機能
RNA結合タンパク質:RNPを構成するタンパク質には、RNAと結合する能力を持つ「RNA結合タンパク質」が含まれます。
芳香族アミノ酸:これらのタンパク質は、RNAと相互作用する芳香族アミノ酸を含むモチーフを持ち、RNA結合を安定化させるリシンの役割も担っています。
細胞の老化防止:通常の細胞が分裂を繰り返すとテロメアが短くなりますが、テロメラーゼがテロメアの長さを維持することで、細胞の老化(複製老化)を遅らせることができます。
幹細胞や生殖細胞の機能維持:
テロメラーゼは、自己の増殖を繰り返す幹細胞(ES細胞、iPS細胞を含む)や、次世代の個体を作る生殖細胞で活性化されています。これにより、これらの細胞は半永久的な増殖を可能にし、組織の機能維持や次世代の形成に貢献します。
テロメラーゼとテロメアの役割
テロメアの機能:テロメアは染色体の末端にある保護構造であり、細胞分裂の際にDNAが失われるのを防ぎ、染色体の構造を維持します。
テロメアの短縮:DNAが複製される際、DNAポリメラーゼは末端を完全に複製できないため、テロメアは短くなっていきます。この短縮が限界に達すると、細胞は分裂を停止し、老化します。
癌細胞においては何がテロメラーゼを活性化させたのでしょうか?癌細胞を生み出したherpesウイルスです。まず癌細胞は幹細胞を持っている細胞しか生まれません。何故ならばすべての癌はヘルペスが感染して核のゲノムDNAに自分のゲノムDNAを組み込み部位特異的遺伝子組み換えを癌関連遺伝子の2種類のドライバー遺伝子変異を起こして癌を生み出すからです。ドライバー遺伝子とは、がんの発生・増殖に直接的かつ中心的な役割を果たす遺伝子の変異のことです。細胞の増殖を促進するアクセル役のがん遺伝子や、ブレーキ役のがん抑制遺伝子の変異などがこれにあたります。これらの変異が細胞の正常な増殖バランスを崩し、がん化を促進します。このようにすべてのherpesウイルスは増殖・分裂できる幹細胞にしか感染して癌関連遺伝子の2種類のドライバー遺伝子変異を起こしてがんを作っているのです。この時にテロメラーゼの活性化は遺伝子異常によって引き起こされ、肝細胞がんでは「テロメラーゼ遺伝子異常」が約70%と非常に高い頻度で発生する重要なドライバー遺伝子異常とされていますがすべての癌細胞は「テロメラーゼ遺伝子異常」は必ずあります。
ドライバー遺伝子異常とは、がんの発生や増殖に直接関与する「ドライバー遺伝子」にherpesによって起こる変異のことで、がん細胞の増殖を促します。このドライバー遺伝子異常を標的とした分子標的薬による治療が近年進んでおり、患者さんごとに異なるドライバー遺伝子を特定し、最適な治療法を選択する「がんゲノム医療」が提供されています。
ドライバー遺伝子とはがん細胞の発生や増殖に直接的な原因として関与する遺伝子です。
細胞を増殖させる「がん遺伝子(アクセル役)」と、細胞増殖を抑制する「がん抑制遺伝子(ブレーキ役)」の両方を含みます。がん細胞にのみみられる変異であり、正常組織には通常見られません。
ドライバー遺伝子異常のメカニズムとはヘルペスによる突然変異によって正常組織に遺伝子異常が蓄積することでがん化が進みます。複数のドライバー遺伝子変異が獲得されることで細胞の増殖が異常になり、がん化に至ります。因みに「ドライバー遺伝子異常」と「パッセンジャー遺伝子異常」の違いについてはドライバー遺伝子変異はがんの発生に直接関わる「運転手」のような遺伝子です。がんの発生とは直接関係ない遺伝子変異を「パッセンジャー遺伝子変異(乗客変異)」と呼びます。
ドライバー遺伝子異常によって引き起こされる主な癌としては、非小細胞肺がん(ALK融合、EGFR、KRAS変異など)、乳がん(HER2など)、大腸がん(KRAS、APC変異など)、膵臓がん(KRASなど)、メラノーマ(BRAF、GNA11など)、肝細胞がん(テロメラーゼ遺伝子異常など)、腎細胞がん(VHLなど)が挙げられます。これらのドライバー遺伝子変異を特定することで、その変異を標的とした分子標的薬による個別化医療が可能となります。
具体的なドライバー遺伝子と関連するがんの例
非小細胞肺がん:
ALK融合遺伝子変異:ALK遺伝子と他の遺伝子が融合することでがん化を促進します。
EGFR変異:特に肺腺がんの約30%にみられるドライバー変異で、この変異を標的とする分子標的薬が開発されています。
KRAS変異:肺がんを含め様々ながんに関与し、KRAS G12C阻害薬が開発されています。
乳がん:
HER2(ERBB2)遺伝子変異:乳がんを含む特定のがんでみられ、HER2を標的とする治療薬が存在します。
大腸がん:
KRAS変異:肺がんと同様に大腸がんの発症にも関与しています。
APC変異:コリバクチン毒素による変異が特徴的で、大腸がん発症の要因となることが示唆されています。
膵臓がん:
KRAS変異が関与するドライバー遺伝子として知られています。
メラノーマ:
BRAF、GNA11、c-KITなどの遺伝子変異が関与しています。
肝細胞がん:
テロメラーゼ遺伝子の異常が約70%の症例で見られ、肝細胞がんの最も頻度の高いドライバー遺伝子です。
腎細胞がん:
VHL遺伝子変異がよく知られており、腎細胞がん発症のドライバー遺伝子の一つです。
ドライバー遺伝子異常と分子標的治療
ドライバー遺伝子変異は、がん細胞の増殖に直接関与しているため、その変異を標的とする分子標的薬による治療が可能です。この「ゲノム医療」とも呼ばれるアプローチにより、特定のがんに対してより効果的で副作用の少ない治療が期待されていますが無駄です。
「ゲノム医療」とは個々の遺伝情報(ゲノム)を基に、病気の原因を特定し、一人ひとりに合った診断や治療を行う医療のことです。特にがんの分野では、がん細胞の遺伝子を網羅的に調べる「がん遺伝子パネル検査」によって遺伝子変異を明らかにし、その変異に効果が期待できる薬(分子標的薬など)を検討する「がんゲノム医療」が普及していますが無駄です。というのは遺伝子変異がなぜ起こったのかを全く理解されていないからです。個々のがん患者に起こった原因はすべてヘルペスが感染した細胞のゲノムDNAの増殖関連遺伝子を突然変異させたからですが個人個人の変異した遺伝子を個々に修復してもヘルペスが生き続け増殖する限り癌を治すことは不可能であるからです。
分子標的治療とはがん細胞に特徴的な分子を標的とし、その働きを阻害する薬(分子標的薬)を用いた治療法です。従来の化学療法ががん細胞と正常細胞を区別なく攻撃するのに対し、分子標的治療薬はがん細胞の特定の分子のみを標的とするため、正常細胞への影響を少なくし、高い効果が期待できるのが特徴です。乳がん治療の「トラスツズマブ」などがその代表例で、さまざまな種類のがんに用いられています。がん細胞の特定の分子などは存在しないので分子標的治療も無駄です。癌の原因はヘルペスが2種類の増殖関連遺伝子を突然変異させて生まれたのですから原因であるヘルペスを退治する以外の治療法は存在しないのです。分子標的治療もゲノム医療もすべて医者の病気つくりの遊びです。しかも一つの細胞に数百個もある2種類の増殖関連遺伝子をすべて調べることは不可能であります。さらにヘルペスが感染した癌になっていない細胞と癌になっている細胞のすべてを調べ尽くすことも不可能です。癌はヘルペスが2種類の増殖関連遺伝子を突然変異させて生まれたことも知らない現代医療の治療方法で癌を治すのは無理なので癌で死んでいくのです。
分子標的薬の標的にされる分子は何でしょうか?
多くの場合、分子標的薬は、変異した癌関連遺伝子から作られた異常なタンパク質などを標的にして、がん細胞の増殖を抑える薬です。遺伝子検査でこの変異が見つかった場合、その変異に対応する分子標的薬が治療の選択肢となります。がん細胞の増殖を抑える本当の薬はヘルペスががん細胞の増殖をもたらしているだけですから分子標的薬も人の命をもてあそぶだけの薬です。
分子標的医療の基本的な仕組み
遺伝子の変異が原因:がんは遺伝子に変異が起こることで発生します。
異常なタンパク質の生成:遺伝子変異により、異常なタンパク質が作られ、これががん細胞の増殖や転移を引き起こします。
標的とするタンパク質:分子標的薬は、この異常なタンパク質を標的としてその働きを抑えることで、がん細胞の増殖や転移を阻害します。しかし癌は治すことはできません。
遺伝子検査の重要性
標的の特定:分子標的薬が有効な場合、まず使用する分子標的薬に対応する遺伝子変異があるかどうかを遺伝子検査で調べます。
がんゲノム医療:遺伝子パネル検査などを用いて多数の遺伝子変異を同時に調べ、その結果に基づいて医療を行うのががんゲノム医療です。これは標準治療の選択肢が限られる場合などに期待されています。
分子標的治療の特徴:原因治療ではないので意味はないのです
ピンポイントな攻撃:
がん細胞の増殖や生存に必要な特定の分子(タンパク質や遺伝子)だけを標的にします。
正常細胞への影響が少ない:
がん細胞と正常細胞の分子的な違いを利用して治療するため、正常細胞へのダメージが少なく、副作用が軽減される傾向にあります。
個別化医療の推進:
患者さんのがんの分子的な特徴を調べ、そのがんの標的となる分子に合った分子標的薬を選択します。
分子標的治療の種類
HER2(ハーツ―)阻害薬:乳がんなどで見られる特定のタンパク質(HER2)を標的とします。
血管新生阻害薬:がんの成長に必要な血管の形成を阻害します。
CDK4/6阻害薬:がん細胞の増殖を促す酵素の働きを阻害します。
免疫チェックポイント阻害薬:免疫細胞ががん細胞を攻撃する際にブレーキをかける分子を阻害し、免疫の働きを活性化させます。
分子標的治療の適応とされているがん
肺がん、乳がん、大腸がん、胃がん、腎臓がん、血液がん、肝臓がんなど、多くの種類のがんの治療に導入されています。
分子標的治療への応用
ドライバー遺伝子変異を標的とする「分子標的薬」の開発が進み、がんの治療に用いられています。患者さんのドライバー遺伝子を解析することで、その方に合った治療法(個別化治療)を選択する「がんゲノム医療」が提供されています。
分子標的治療の今後の展望
全ゲノムシークエンス技術の進歩により、これまでにない新規のドライバー遺伝子や複雑なゲノム構造異常の解析が可能になっています。ドライバー遺伝子異常の解析は、がんの予防や早期発見にも今後ますます活用されると期待されていますが、原因治療ではないので医者と製薬会社が人を殺してもうかるだけです。言うまでもなく癌という病気はこの世にはありません。ない病気は治すものではないのです。
幹細胞と生殖細胞とテロメアの短縮
生殖細胞は次世代に遺伝情報が正しく受け継がれるために、テロメアの短縮を防ぎます。
幹細胞(ES細胞、iPS細胞など)は半永久的に増殖・分化する必要があるため、テロメアが短くならないようにテロメラーゼが働いています。がん細胞は異常な増殖を続けることで、腫瘍を形成します。テロメラーゼの活性化が、がん細胞の無限増殖(不死化)の大きな要因となっています。
テロメラーゼの機能には一つ目にはテロメアの伸長がありDNA複製時に短くなるテロメアに、特徴的な塩基配列(ヒトでは「TTAGGG」)を付加し、テロメアの長さを維持します。二つ目には細胞老化の抑制ですがテロメアが一定の短さに達すると細胞は分裂を停止(老化)しますが、テロメラーゼによってテロメアの短縮が防がれるため、幹細胞や生殖細胞や癌細胞では半永久的に分裂を繰り返せます。
テロメラーゼと疾患の関わりは特に癌との関りは多くのherpes感染による増殖関連遺伝子の変異が作り出したがん細胞で異常になったテロメラーゼの活性が高まっており、細胞が不死化して無限に増殖することが可能になります。その他のテロメラーゼの機能不全の疾患には、先天性角化異常症などの疾患を引き起こすこともあります。
ヘルペス感染が細胞に起こった時にどの様にherpesウイルスは感染細胞のゲノムDNAに入り込んで癌関連遺伝子(増殖関連遺伝子)を癌化するのか?まずがん細胞はもともと幹細胞であり幹細胞は増殖・分裂するときに46本の染色体をDNA(遺伝子)の複製のために92本の1倍体の染色体にばらばらになります。92本の1倍体の染色体にばらばらになるときにherpesウイルスは細胞のゲノムDNAに自分のゲノムDNAを組み込み細胞のゲノムDNAの遺伝子を組み替えてしまい、がん関連遺伝子を突然変異させてしまうこともあるのです。
幹細胞やがん細胞にテロメラーゼが存在し続けるのは、幹細胞が生み出されるべき子供の細胞を維持・供給し、がん細胞は無限に増殖し続ける必要があるためです。テロメラーゼは、細胞分裂のたびに短くなる「テロメア」という染色体末端の構造を修復する酵素であり、この酵素の働きによって細胞は老化せず、分裂を続けることができます。
テロメラーゼが幹細胞に存在する理由は幹細胞は、将来的に体をつくるさまざまな細胞に分化する能力を持っています。テロメラーゼが働くことでテロメアの短縮を防ぎ、幹細胞が何度も分裂してもその能力を維持できるため、体を作り続けることができます。
テロメラーゼががん細胞に存在する理由はがん細胞は異常な増殖能力を持っており、その「不死化」(無限増殖)はテロメラーゼの活性化によって支えられています。細胞が分裂するたびにテロメアは短くなりますが、テロメラーゼが活性化するとテロメアが再生・修復され、細胞は分裂回数の制限を超えて増殖し続けることができるようになります。
テロメラーゼの基本的な働きはテロメアは、染色体の末端を保護する役割を持つDNAの構造です。細胞がDNAを複製する際に、末端のテロメアが完全に複製されずに短くなっていきます。テロメラーゼは、この失われたテロメアの配列を補うことで、テロメアの長さを維持します。
ヘイフリック限界と老化との関り
正常な細胞が分裂回数に上限を持つことを指すのに対し、がん細胞はテロメアの維持などにより、分裂回数の上限(ヘイフリック限界)を乗り越えて無限に分裂する能力を持つ点が異なります。正常細胞の分裂停止は、染色体末端のテロメアが短くなることによる一種のプログラムされた老化であり、DNA損傷の修復不可能な状態の緊急事態を防ぎ、がん化を防ぐ役割もあります。
ヘイフリック限界とは
正常細胞には分裂できる回数に限界があり、この現象を「ヘイフリック限界」と呼びます。染色体の両端にあるテロメアが、細胞が分裂するたびに短くなり、限界に達すると細胞は分裂を停止し、老化状態になります。
テロメアが短くなりすぎると、細胞周期が停止するタンパク質が作られ、分裂ができなくなります。
がん細胞とヘイフリック限界
正常細胞とは異なり、がん細胞にはこの分裂回数の上限がありません。
がん細胞では、テロメアを長く保つ「テロメラーゼ」という酵素がヘルペスによって異常に活性化しています。
異常になったテロメラーゼがテロメアを常に修復・伸長させることで、がん細胞はヘイフリック限界を無視し、無制限に増殖し続けることができます。
細胞の老化とがんの関わり
正常細胞がヘイフリック限界に達して老化することは、がん遺伝子が活性化した細胞を分裂させないようにする、一種の防衛機構でもあります。
細胞周期の制御に関わる遺伝子(p53、p16など)が損傷し、この制御機構が破綻すると、がんが発生しやすくなります。p53とはがん抑制遺伝子の一種で、「ゲノムの守護者」と呼ばれる重要なタンパク質です。細胞がDNA損傷などのストレスを受けた際に、細胞周期を停止させてDNAの修復を促したり、修復が不可能な場合は細胞死(アポトーシス)を誘導したりすることで、がん化を防ぐ役割を担っています。p16とは細胞の増殖を抑制し、がんの発生を予防するがん抑制タンパク質を指します。p16とは細胞周期のG1期からS期への移行を停止させる働きを持ち、過剰な細胞増殖を抑え細胞を老化させることで、生体防御機構として機能します。p16遺伝子に変異が生じると、この機能が失われ、がんの発生リスクが高まります。また、子宮頸がんや中咽頭がんなどにおいて、HPV感染の指標となるなど、診断の補助としても利用されます。
herpesウイルスが生み出した異常ながん細胞はこの制御をすり抜けるため、無制限に増殖できるのです
テロメラーゼと癌関連遺伝子
テロメラーゼは、細胞の染色体末端(テロメア)を伸長させる酵素で、多くのがん細胞で異常になったテロメラーゼは活性化し、テロメアを維持することで不死化(無限の増殖能力)を可能にします。テロメラーゼの活性化はヘルペス性遺伝子異常によって引き起こされ、肝細胞がんのみならずあらゆる種類の癌では「テロメラーゼ遺伝子異常」が見られます。あらゆるherpesによって生まれた癌細胞のテロメラーゼはherpesのため異常になっているのでこのテロメア機能も維持されているのです。
テロメラーゼとテロメア
テロメア:
染色体の末端にある遺伝情報を持たないDNA構造で、染色体を保護する役割を担っています。
老化細胞が分裂する際にDNAの両端(テロメア)がうまく複製できず、徐々に短くなって癌が起こる前に細胞の老化をもたらします。
テロメラーゼ:
DNAの末端を伸長させることで、細胞が老化するまではテロメアの短縮を防ぐ酵素です。
がん細胞での異常なテロメラーゼの働き
細胞の不死化:
多くのがん細胞ではherpesがテロメラーゼの遺伝子を変異させてしまい再活性化し、テロメアの短縮を防ぎます。これにより、がん細胞は無限に増殖する能力(不死化)を獲得します。
遺伝子異常との関連:
Herpesによって突然変異したテロメラーゼ遺伝子の発現が際活性化すると、細胞のテロメアが維持され、がん細胞の増殖が可能になります。
ヘイフリックの限界の発見と老化
ヘイフリックの限界の発見は、細胞の老化メカニズムの解明や、がん研究の発展に大きく貢献しました。細胞の寿命には限界があるという事実から、生物の寿命のメカニズムを理解する上での重要な手がかりとなっています。
細胞老化と“P53”という遺伝子
細胞老化のカギを握っているのが“P53”という遺伝子でありかつ、“ゲノムの守護神”との異名を持っており、損傷したDNAの修復や細胞分裂の調整などにも携わっているという特異な遺伝子なのです。傷ついたDNAを修復する一方で、修復できないほどにDNAがダメージを受けた場合には、細胞の老化をうながし、老化細胞として排除する。まさにゲノムの守護神、正常な細胞を守る司令塔といえるでしょう。というのも、老化細胞は、異常な増殖を繰り返すがん細胞を、その周囲の細胞とともに老化させて、増殖を抑え込むという役割も果たしているからです。繰り返しになりますが、老化細胞はもう細胞分裂しません。増殖しない細胞です。がん細胞を老化させることによって、その異常増殖を防ぐ、つまりヘルペスによって生まれたがんを防ぐことが老化細胞のプログラムのひとつなのです。
老化とは、成熟期以降に誰にでも起こる生理機能の低下で、遺伝的要因と生活習慣などの環境要因が関与して進行します。時間経過(加齢)は避けられませんが、老化のスピードには個人差があり、生活習慣の工夫によって遅らせることが可能です。体力や記憶力の低下、シワや白髪の増加など、様々な身体的変化として現れます。
老化の主な原因
活性酸素による酸化ストレス:呼吸や紫外線、ストレスなどによって発生する活性酸素は、細胞や遺伝子を傷つけ、体の機能低下を引き起こします。
糖化:
ブドウ糖が体内のタンパク質や脂肪と結合し、機能を変質させる現象で、皮膚のコラーゲンや眼のレンズが褐色化・白濁する原因となります。
老化のスピードと遺伝的要因と環境要因:
遺伝的な素質に加え、食生活や運動不足、ストレスなどの生活・環境要因が老化のスピードに影響を与えます。
加齢と老化の違い:
「加齢」は単なる時間の経過を指しますが、「老化」は加齢に伴う身体・精神機能の低下そのものを指します。
老化のスピードの個人差:
老化の進行速度は人によって異なり、生活習慣の改善などによって遅らせることが可能です。
老化の段階的な変化:
40歳代頃から老化のスピードが加速すると言われており、体力や心臓機能、肺機能など全身の生理機能が徐々に低下します。
老化の具体例
身体の見た目の変化:顔のしわ、肌のハリ不足、髪の白髪など。
身体機能の低下:脳神経系の機能低下による認知機能の低下、心血管系の機能低下、肺活量の減少など。
骨や関節の変化:骨粗鬆症や関節炎などが引き起こされることがあります。
老化が癌の原因ではないデータをお見せします。2025年 最新・世界平均寿命ランキングと2023年 がん死亡率の二つのデータを自分でじっくり見て世界の国の平均寿命と2023年の世界の国々がん死亡率を見て比べて中川恵一先生の「癌は老化による病気であるか」について考えてください。
2025年 最新・世界平均寿命ランキング
WHO発表のデータから、世界185か国の平均寿命をランキング形式でまとめた(男女合計)。
順位 国名 平均寿命
1位 日本 84.46歳
2位 シンガポール 83.86歳
3位 大韓民国 83.80歳
4位 スイス 83.33歳
5位 オーストラリア 83.10歳
6位 ノルウェー 82.88歳
7位 ルクセンブルク 82.78歳
8位 スペイン 82.66歳
9位 スウェーデン 82.66歳
10位 アイスランド 82.58歳
11位 イタリア 82.20歳
12位 ニュージーランド 82.20歳
13位 フランス 81.92歳
14位 キプロス 81.91歳
15位 マルタ 81.81歳
16位 イスラエル 81.74歳
17位 アイルランド 81.60歳
18位 カナダ 81.58歳
19位 フィンランド 81.53歳
20位 ベルギー 81.51歳
21位 デンマーク 81.18歳
22位 ポルトガル 81.18歳
23位 オランダ 81.12歳
24位 オーストリア 80.99歳
25位 ドイツ 80.49歳
26位 スロベニア 80.41歳
27位 イギリス 80.10歳
28位 プエルトリコ 79.90歳
2023年 がん死亡率
順位 国名 単位:人/10万人 注
1 ハンガリー 275.00
2 クロアチア 267.70 2
3 スロベニア — 以下会員限定 —
4 ラトビア
5 スロバキア —
6 ポーランド —
7 リトアニア —
8 デンマーク —
9 イギリス —
10 アイルランド —
11 チェコ —
12 オランダ —
13 ルーマニア —
14 エストニア —
15 ロシア —
16 ギリシャ —
16 アイスランド —
18 フランス —
19 ポルトガル —
20 ドイツ —
21 ブルガリア —
22 カナダ —
23 オーストラリア —
24 イタリア —
25 ノルウェー —
26 オーストリア —
27 ベルギー —
28 スペイン —
29 チリ —
30 米国 —
31 日本
世界一癌が多い国はどこですか?
世界一癌が多い国は特定されておらず、国や調査対象によって指標が異なるため、明確な答えはありません。しかし、日本は先進国の中で癌による死亡者数が増加する例外的な国であり、国民の約半数が一生のうちに癌になる「がん大国」と言われます。一方で、早期発見率と治療が進む富裕国では、死亡者数よりも罹患者数(がん患者数)が多くなる傾向があります。
「がん大国」と言われる日本の状況
①死亡者数の増加:日本は先進国の中で、がんによる死亡者数が年々増加している数少ない国の一つです。
②罹患者数:2人に1人が一生のうちにがんになる、3人に1人ががんで死亡するという割合は世界一と言えます。
③死因第1位:がんは日本人の死因の第1位となっており、1981年以降、脳卒中を抜いて1位の座を維持しています。
「世界一」の定義の項目が複数ある理由
①罹患率と死亡率:cancer (がん)の「多さ」を測る場合、癌にかかる人の数(罹患率)を指すのか、それとも癌で亡くなる人の数(死亡率)を指すのかで指標が異なります。
調査方法や期間:どの期間のどの国を対象に調査したかによって結果が異なるため、世界で最も癌が多い国を一つに特定するのは困難です。
②医療の発展度:医療が発展し、がんの早期発見と治療が可能な富裕国では、発見率と生存率が高くなるため、罹患者数(がんにかかっている人の数)が多くなる傾向があります。
このように、日本は「がん大国」というべき状態ですが、世界全体で最もがんが多い国がどこかということは、指標によって異なるため、断言することはできません。
中川恵一先生の「癌の秘密」のすべての論拠が間違っていることを証明し続けていきます。
黒字は主に中川先生の論文であり赤字は主に私の癌に対する理論であり、中川先生の間違いを指摘する反論文です。
私たちのカラダの細胞は、60兆個の細胞からなっています。毎日数千億から1兆個の古い細胞が死にますので、細胞分裂をして、減った細胞を補う必要があります。これが細胞の新陳代謝です。古くなった細胞と新しい細胞を入れ替える新陳代謝で一番大切なのは細胞の核にある二重らせん構造の染色体のDNAを2倍にして同じ細胞を2個作ることです。これを細胞の増殖・分裂と言います。この細胞分裂の時にherpesは染色体のゲノムDNAに自分のゲノムDNAを入り込ませることができるのです。なぜ細胞の増殖・分裂の時に自分のゲノムDNAを入り込ませ入れ替えることができるのでしょうか?
細胞の染色体は物理的にも化学的にも極めて安定しており、この新陳代謝の新旧の細胞の入れ替えの時にまずDNAの複製が行われるので46本の凝縮した隙間の無い染色体が分裂してばらばらの姉妹染色分体の92本になるので、このバラバラになった92本の染色体の間に隙間ができherpesが自分のゲノムDNAをばらばらの姉妹染色分体の92本に自由自在に組み込むことが可能になり細胞のDNAと入れ替えてしまい、DNAでできた遺伝子の組み換えを行って細胞の遺伝子を突然変異させ、癌のみならず後天的なあらゆる病気を生み出してしまうのです。
例えばゲノム組み込みはEBVと同じように、HHV-8のゲノムが宿主細胞のゲノムに組み込まれて癌が生まれるのは宿主細胞のゲノムにヘルペスウイルス自身のゲノムDNAが一つの細胞に数百個もある2種類の増殖関連遺伝子のどれかに覆いかぶさり宿主細胞のゲノムの増殖関連遺伝子と入れ代わる結果、増殖関連遺伝子の突然変異を生み出して異常なタンパクが作られてしまうのです。異常なタンパクが生まれるのはヘルペスウイルスが自分のDNAと宿主のDNAと入れ替えてしまうのでいくつかの遺伝子も入れ替わるのは当たり前のことなのです。herpesと宿主細胞のDNA間同士の入れ替わる現象は単純に「DNA入れ替え(replacement)」の結果、特定の蛋白質の設計図である遺伝子が突然に変異してしまい異常なたんぱく質を生み出してしまうのです。たまたま、この変異した遺伝子が2種類の増殖関連遺伝子であれば1個の癌細胞(増殖関連細胞)に過ぎないのです。この遺伝子の入れ替わりはヘルペスがあらゆる細胞に感染した後、宿主のゲノムDNAに潜伏感染するときに見られる極めて普通のことなのです。最も多くの原因不明の遺伝子病はこのようにヘルペスがherpesと宿主細胞のDNA間同士の入れ替わる時に生ずるのです。
細胞分裂では、細胞の設計図であるDNAを正確にコピーする必要があります。細胞の設計図は遺伝子でありDNAではありません。DNAはあくまでも遺伝子を載せている物質であり蛋白を指定する情報ではないのです。DNAと遺伝子の関係はDNAは巨大な分子ですが、そのすべての塩基配列に意味があるわけではありません。DNAの中で、特定の機能を持つタンパク質を作るための情報が書かれている部分を「遺伝子」と呼びます。人間の場合、遺伝子はDNA全体のわずか1%程度にしかすぎず、残りの部分の役割については今も研究が続けられているのです。DNAコピーミスが細胞の中川先生は間違いだらけです。突然変異ではありません。突然変異するのは遺伝子であって細胞の突然変異は存在しません。人間のすることですから、コピーミスを起こすことがあります。人間のすることと細胞のコピーミスとは全く関係がありません。DNAを正確にコピーできなくても物質であるDNAはDNA修復機構が100%修復できます。細胞の突然変異という概念は医学にはありません。
癌細胞が生まれるのは2種類の増殖関連遺伝子に突然変異が起こるときだけなのです。
しかも遺伝子情報を担っているゲノムの遺伝子を修復できるシステムを細胞のみならずDNA修復機構は持ってはいません。細胞は遺伝子を損傷から回復させるための「ゲノム修復システム」を自然に持っていますが、このシステムは万能ではなく、細胞自身が設計図を元に「設計図自体を根本的に書き換える」ことはできません。DNAと遺伝子の関係はDNAは巨大な分子ですが、そのすべての塩基配列に意味があるわけではありません。DNAの中で、特定の機能を持つタンパク質を作るための情報が書かれている部分を「遺伝子」と呼びます。人間の場合、遺伝子はDNA全体のわずか1%程度にしかすぎず、残りの部分の役割については今も研究が続けられています。
いいえ、細胞は「遺伝子修復機構」という独立した機構を持つのではなく、「DNA修復機構」を用いて、ゲノム(DNA)を構成する遺伝子の損傷を修復していますが遺伝子の損傷を直接修復することはできません。あくまでも当たらぬも八卦、当たるのも八卦の世界です。このDNA修復機構はDNA損傷のタイプに応じて様々な仕組み(塩基除去修復、ヌクレオチド除去修復、相同組換え修復など)で働き、遺伝情報を正確に維持するためではなくDNAという遺伝物質の修復に不可欠なプロセスに過ぎないのです。決して遺伝子情報を修復することではないのです。
一方、遺伝子は遺伝子情報そのものであると同時に即遺伝子情報を発現してタンパク質を作らせる情報そのものなのです。この遺伝子情報の間違った発現が異常なタンパクを作らせてしまい癌細胞(増殖過剰細胞)が生まれることになるのです。傷ついたDNAが遺伝子が生み出す異常な蛋白質を作らせて癌細胞(増殖過剰細胞)を作ることができますか?不可能です。遺伝子の突然変異こそ癌細胞の誕生となるのですがDNAの突然変異はあり得ないことなのです。何故ならば突然変異とは、特定の蛋白を指定する増殖関連遺伝子そのものを突然変異させたヘルペスウイルスが生み出した突然変異の結果なのです。血管生物の持つDNA(核酸)が物理的・化学的要因や複製ミスなどによって質的・量的に変化し、遺伝形質に変化が生じる現象、またはその変化自体のことです。
遺伝子突然変異(Genetic mutation)と変異(mutation)の違いとは何でしょうか?
「変異(へんい)(mutation)」は遺伝子情報が変化する漠然とした現象全般を指します。特定の形質を指定するタンパク質の変化ではありません。生物の形態や性質が漠然と変化する現象を広く「変異」と呼びます。一方、「遺伝子突然変異(Genetic mutation)」は特定の遺伝子が変化して異常な蛋白質が作られることです。「遺伝子複製時に間違いなどが起こり個別の正しい遺伝子の発現となる正常なタンパクが作れなくなる現象」を指します。その変化の「原因」が遺伝子の変化ある場合に、その現象を「突然変異」と呼びます。「遺伝子複製」という言葉は、厳密な専門用語としては間違いです。一般的には「DNA複製」と呼ぶべきです。
「DNA複製」と使われるべき理由は生物の遺伝情報は、DNAという物質に記録されています。遺伝子の物質としての本体もこのDNAですが遺伝子と違って特定の蛋白を指定することはできないからです。そのため、細胞分裂の前に遺伝情報全体を正確にコピーする過程は、DNAそのものを複製するという意味で「DNA複製」と呼ばれます。細胞は「遺伝子複製」を行うシステムは持っていないのです。
細胞はDNA複製を結果的に行う「遺伝子複製」のシステムは持っていますが目的的な個別のシステムとして独立した「遺伝子複製」だけのシステムは持っていませんのは何故でしょうか?
細胞は、個々の遺伝子だけを選んで複製する独立したシステムは持っていません。
DNA複製が「結果的に」遺伝子複製を行う理由
遺伝子とDNAの関係: 遺伝子とは、DNA分子の中にある、タンパク質などの設計図となる特定の領域(配列)のことです。DNA全体は、遺伝子領域だけでなく、機能がまだ不明な部分や、遺伝子の発現を制御する領域など、さまざまな配列で構成されています。
DNA複製の対象: 細胞が増殖するためにDNAを複製する場合、それは特定の遺伝子だけをコピーするのではなく、DNA分子全体をまるごとコピーするプロセスです。これによって、ゲノム全体に含まれるすべての遺伝情報が、新しい娘細胞に正確に受け継がれます。
目的と手段: 細胞の最終的な目的は、細胞全体を正しく増殖させることであり、そのためにゲノム全体を複製する必要があります。個々の遺伝子を単独で複製するのではなく、DNA全体を複製するという手段をとることで、必然的にすべての遺伝子も複製されることになります。
例外的なケースと「個別」の概念
転写(発現): 遺伝子を「コピー」するプロセスには、別のものがあります。それは、DNA上の特定の遺伝子領域から、一時的なメッセンジャーRNA(mRNA)を合成する転写です。これは、細胞がその時々に必要なタンパク質を作るための、まさに「個別の遺伝子情報を取り出す」システムです。
プラスミド: 多くの細菌は、主となるゲノムDNAとは別に、プラスミドという小さな環状のDNAを持っています。プラスミドは、ゲノムDNAとは独立して複製されることがあり、このプラスミド上に含まれる遺伝子は、個別に複製されると言えます。ただし、このシステムもやはり「DNA」を複製しているのであり、細胞内の普遍的なシステムではありません。
結論
細胞は、個々の遺伝子を独立して複製するための「遺伝子複製システム」は持たず、細胞分裂時にゲノムDNA全体を複製するシステムを持っています。その結果として、すべての遺伝子が複製されるのです。遺伝子を「個別に」扱うシステムは、複製ではなく、遺伝子発現(転写と翻訳)という全く別のプロセスになります。
変異(Mutation)
広範な意味合い:遺伝子情報が変化することを指す、より広い概念です。
具体例:
「変異株」は、ウイルスなどの遺伝情報が変化した「集団」を指し、この集団全体が「変異」していると言えます。生殖細胞で起こった遺伝子の変化も、子孫に受け継がれる場合も「変異」と呼びます。
日本語の使い分け:日本人類遺伝学会では、この広い意味の「変異(mutation)」を単に「変異」と呼んでいます。
遺伝子の突然変異(Genetic Mutation)
メカニズム:ヘルペスが宿主の染色体のDNAに自分の染色体のDNAを組み入れこむときに偶然に蛋白を指定する遺伝子と入れ替わる時に元の遺伝子をヘルペスのDNAにかぶされ除去されてしまうので元にあった宿主の正常な遺伝子が消えてしまうので本来の宿主の正常な遺伝子が指定するタンパク質が発現できなくなり、異常な遺伝子が指定する異常なタンパクが生まれてしまうのです。
これを医学界ではDNAの突然変異といわれていますが間違いです。何故ならばDNAが蛋白を指定するのではなくDNAは単にすべての遺伝子を作る材料に過ぎないので特定の遺伝子でもなく従って特定の蛋白質を発現させることもできないからです。仮にDNAが損傷しても100%修復できますが遺伝子の修復は100%不可能です。というのは遺伝子のチェックポイント言う監視機構は細胞は持っていないからです。替える時に複製される際に、一部に読み間違いや組み換えが起こる現象そのものを指します。つまりDNAの突然変異は存在しないのです。突然変異という言葉は「遺伝子突然変異」しか存在しないのです。
遺伝子の突然変異(Genetic Mutation)の結果:遺伝子情報が一部変化し、それによって生物の形質(性質)が変化することになるのです。
遺伝子の突然変異(Genetic Mutation)の例:
DNAの塩基の一つが別の塩基に置き換わる分子レベルの変化や、染色体の構造が変化するなどの、さまざまな程度の変化が遺伝子に偶々「遺伝子突然変異」にでることがあります。
厳密な突然変異と変異の違い
「突然変異」と「変異」は、ほぼ同じ意味で使われることが多い言葉ですが、厳密には以下のようなニュアンスの違いのみならず本質的な違いが一つあります。癌は「遺伝子の突然変異」で起こる病気であり決して「DNAの突然変異」で起こる病気ではないことだけはよく覚えてください。
| 遺伝子突然変異 (genetic mutation) | 変異 (variation / mutation) | |
| 定義 | 遺伝子の塩基配列や染色体の構成が、突然、永続的に変化すること。突然変異によって生じた遺伝子の変化は、子孫に遺伝する場合があります。 | DNAや遺伝子の構成が、質的・量的に変化すること。 広義には、遺伝する「突然変異(mutation)」も、世代間で遺伝しない「環境変異(variation)」も、すべて「変異」に含まれる。 |
| 語源 | 英語の「mutation」に、「突然」という日本語の言葉を加えて訳されたもの。 | 英語の「variation」または「mutation」に対応する。 |
| 学術用語 | 現在の遺伝学では、「突然」という言葉が不適切であるとして、単に「変異(mutation)」と呼ぶことが多い。 | 「変異(mutation)」が、突然変異の過程そのものを指す学術用語として使われることが多い。 |
| 例 | * 点突然変異: DNAの塩基配列が1つだけ変化する。 * 染色体突然変異: 染色体の構造や数に変化が起こる。 | * 遺伝子の変異(mutation): 親から子に遺伝する変化。 * ウイルスの変異(mutation): ウイルスの増殖に伴う遺伝子変化。 * 環境変異(variation): 生まれた代の個体のみに現れ、遺伝しない変化。 |
厳密な突然変異と変異の違いの要約
遺伝子突然変異は、遺伝子の構成が突然かつ永続的に変化する「事象そのもの」を指します。
変異は、遺伝子やDNAの変化を指す広範な言葉で、「突然変異」も「環境変異」もすべて含まれます。
現在では、学術的な文脈で「突然変異」という代わりに「変異」という言葉が使われることが多くなっているのでDNAの突然変異という紛らわしい言葉が生まれるのですが医学者でない限り「遺伝子変異」も「遺伝子突然変異」も「DNA変異」も「DNA突然変異」も「突然変異」も「変異」も同じだと考えても許されます。
変異は英語では variationと mutation)があります。Variationと mutationの違いは何でしょうか?Variationはより広範な「多様性」を指し、MutationはDNAの具体的な「変化」を指します。
このように、VariationとMutationは混同されやすいですが、それぞれ異なる概念を表す言葉です。
Variationは「多様性」や「差異」、Mutationは「変異」や「突然変異」を意味し、遺伝学用語として区別されます。Variationは遺伝的な違いそのものを広く指し、MutationはDNA配列に生じる具体的な変化(突然起きた変化)を指すニュアンスがありますといわれますが医学英語ですからニュアンス(微妙な意味合いや違い)は排除すべきですね。
Variation(バリエーション)は多様性と訳してもよいでしょう。
意味:物事の変化や、個体間に見られる多様な違いのこと。
Variation(バリエーション)の使われ方:生物全体や集団の形質や遺伝子の多様性を表す際に使われます。集団や種の中の個体間における遺伝子の違いを指します。
例:人間の瞳の色や体質、病気のかかりやすさなど、個人差として現れる多様な違い全体を指します。人間集団における、目の色、髪の色、身長などの違いは、遺伝的変異(genetic variation)の現れです。突然変異(mutation)が、変異(variation)の最も根本的な原因となります。
意味:遺伝物質(DNAやRNA)に生じる質的または量的な変化のこと。日本語では「突然変異」とも訳されますが、現在では「突然」という言葉は適当ではないと考えられ、「変異」が広く使われています。何故ならば「突然変異」は「遺伝子突然変異」にのみに用いるべきであるからです。
Mutation(ミューテーション)の使われ方:DNA配列が変更される具体的なプロセスを指す際に使われることがあります。個々の細胞のDNA配列に生じる永続的な変化です。
例:DNAの塩基が入れ替わるSNP、塩基配列が挿入されたり欠失したりするindel(インデル)など、具体的なDNAの変化を指します。indel(インデル)とは遺伝学における塩基配列の「挿入(Insertion)」と「欠失(Deletion)」の頭文字を取ったもので、DNAの塩基が抜け落ちたり、新たに挿入されたりする変異のことです。これらの変異はゲノムの多様性を生み出し、遺伝子の機能に影響を与える可能性があり、疾患や進化において重要な役割を果たします。
「多型(polymorphism)」とは
突然変異(mutation)が個々の遺伝子に起こるDNA配列の変化を指すのに対し、変異(variation)は、集団全体に見られる遺伝的な違い、つまり多様性を指す、より広義な概念です。
かつては病気の原因となる変化を「突然変異(mutation)」、病気と関連しない一般的な集団内の違いを「多型(polymorphism)」と区別することがありましたが、明確な線引きが難しく、差別的と見なされる可能性もあるため、近年では、両者を含むDNAの変化を「バリアント(variant)」と呼ぶことが推奨されています。
変異は細胞内で発生するもの(体細胞変異)と生殖細胞で発生し子孫に伝わるもの(生殖細胞系列変異)があり、遺伝子レベル(塩基配列の変化)と染色体レベル(構造や数の変化)で起こります。自然発生的に起こる場合と、放射線や紫外線、化学物質などによって人為的に誘発される場合があり、生物の進化の原動力となり多様性を生み出す一方で、がんや遺伝性疾患の原因となることもあります。
突然変異の種類
遺伝子突然変異:DNAの塩基配列が置換、挿入、欠失などによって変化し、遺伝子の機能が直接変化するものです。
染色体突然変異:染色体の構造や数が変化するものです。
突然変異の原因
自然発生的:細胞分裂や増殖時のDNA複製エラーなど。
外的要因(変異原):紫外線、放射線、特定の化学物質ウイルス感染など
突然変異の影響
進化の原動力:新しい形質を持つ個体を生み出し、生物の多様性と適応性を高めます。
形質への影響:
形質に変化がない場合もある。
健康に悪影響を及ぼす場合(がん、遺伝性疾患など)。
有利な形質となり、進化につながる場合もある。
世代への伝達:生殖細胞に生じた突然変異は子孫に遺伝しますが、体細胞に生じた変異は基本的に遺伝しません。
突然変異とは、生物の遺伝情報を伝えるDNAの塩基配列や染色体の構造、あるいは数の変化が起こることです。と言われていますが親とは異なる新しい形質が突然生じ、それが子孫に遺伝する現象を指します。
進化と突然変異の関係は、進化の原動力となる重要な要素です。
偶然の産物: 突然変異は、生物の生存に有利か不利かに関係なく、ランダムに発生します。
自然選択: 発生した変異のうち、生存や繁殖に有利な形質を持つ個体は子孫をより多く残し、不利な形質を持つ個体は淘汰されます。この自然選択のプロセスを経て、新しい種が生まれることがあります。
がんの遺伝子治療で癌を治すことはできません。何故治せないのでしょうか?がんの原因となる「遺伝子の異常」に直接働きかけ、正常な「がん抑制遺伝子」をがん細胞に導入することで、がんの増殖を抑えたり、がん細胞を自滅(アポトーシス)に導いたりする治療法です。正常細胞への悪影響が少なく副作用が軽いことや、体力の衰えた患者さんでも治療を受けられる可能性があることが特徴ですが、実用化に向けて研究が進められている段階の遺伝子治療はやめるべきです。「遺伝子の異常」を起こした原因はヘルペスであることを知らずして行われるがんの遺伝子治療はすべて対症治療に過ぎないのですべて癌を完治させることができないので100%無駄です。癌の根本完治を目指す治療はヘルペスは殺すことは不可能ですからヘルペスを増やさないことしかないのですからがんの遺伝子治療はすべて対症治療とならざるを得ませんから実用化に向けて研究が進められている段階であるにしろ完成されたとしても癌を直すことができないので患者の苦痛と高額な医療費となりますからすぐにやめるべきです。
細胞は「遺伝子修復機構」という独立した機構を持つのではなく、「DNA修復機構」を用いて、ゲノム(DNA)を構成する遺伝子の損傷を修復していると言われますがこの文章は逆転しています。正しくは「DNA修復機構」を用いて、遺伝子を構成しているゲノム(DNA)の損傷を修復しているだけで遺伝子を修復しているわけではないのです。「DNA修復機構」というのはゲノムDNA(染色体)は細胞のDNA修復機構は決して癌を起こす突然変異を起こした増殖関連遺伝子(癌関連遺伝子)を修復するつもりは何も持ち合わせているわけでもないし目的的に行うシステムも持ち合わせていないのです。「DNA修復機構」に治されたDNAの配列がたまたま増殖関連遺伝子(癌関連遺伝子)の配列が異常な部分だっただけの偶然出会っただけなのです。それがたまたま増殖関連遺伝子(癌関連遺伝子)の配列の異常な部分だったので正常に戻った遺伝子が命令した蛋白が正常に戻っただけなのです。
従って癌細胞をDNA突然変異疾患とか増殖関連遺伝子突然変異疾患というよりも増殖蛋白突然変異症という方がはるかに的をついた病名なのです。何故ならば増殖関連遺伝子を突然変異させて正常な増殖の役割を持っていた細胞の作る蛋白を異常にして生まれた癌細胞は異常なタンパクを作り続ける限り癌を作り続けることになるからです。
ここで原点に戻って考えると正常な蛋白ではなく何が異常な癌蛋白を作らせたのかというと正常な増殖関連遺伝子のヌクレオチドの配列を異常にした原因はいろいろありますが最終的にDNAのヌクレオチドの配列は何によって決められたのでしょうか?遺伝子のヌクレオチドという物質を作るのは誰なのでしょうか?さらにこのDNAという染色体のヌクレオチドの並びが異常になればDNA修復システムがほとんど100%修復できますし、DNAの損傷が長年蓄積してしまって増殖関連遺伝子に突然変異が起きることはないのです。何故ならば細胞分裂のたびごとに細胞周期の厳しいチェックポイントの監視機構が見張っていますから必ず修復すべきDNAは100%修復しますし、修復できない細胞があればアトポーシスという奥の手を使ってその細胞を計画的に殺してしまいます。つまり細胞の一部であるDNAの損傷を修復できなければ大掛かりな細胞もろともDNAの無きものにしてしまうのでDNAの損傷の100%消えてしまうのでDNAの損傷は100%修復できると言っているのです
一方、正常な蛋白質を作るのは変えてはならないヌクレオチドの遺伝子の絶対的な命令であるので変えてしまうと遺伝子病が生まれてしまうのです。癌も特定のヌクレオチドの配列で決められた癌関連遺伝子の変異のために異常な蛋白質ができてしまいこの異常な蛋白質が無限に増えて行く癌細胞を作って最後に癌で死んでしまうのに何故DNAシステムには手に負えない遺伝子修復システムを細胞は持っていないのでしょうか?言うまでもなくDNAも遺伝子も素材としては同じヌクレオチドから作られたのですよ。何故遺伝子の修復システムがなぜ存在しないのでしょうか?
この疑問に対する答えは二つあります。一つ目は癌細胞はヘルペス性感染症ですから感染症は免疫の仕事であって免疫にまかしているのですがherpesは免疫で殺しきれない上に細胞のゲノムDNAに入り込んで隠れてしまうのに加えて、免疫が強い時には極めて賢いherpesは増えることもしないし、細胞の外に出ることもしないので細胞の外でしか免疫は働かないのでherpesは免疫が強い時にはゲノムDNAに潜伏感染で隠れ続けるのです。
二つ目は細胞のDNA修復機構はherpesによって突然変異を起こされてしまった増殖関連遺伝子(癌関連遺伝子)が発現させた異常な癌を起こす蛋白を修復しているわけでもないのです。異常なDNA損傷のタイプに応じて様々な仕組み(塩基除去修復、ヌクレオチド除去修復、相同組換え修復など)で働くことは可能であるのですが、DNA修復機構は遺伝物質を修復ことはできるのですが蛋白を正常に作ってくれる遺伝情報を正確に維持することのできる遺伝子の配列の突然変異を修復できるシステムは持っていないのです。つまりDNA修復機構は「癌は癌関連遺伝子がヘルペスによって損傷して生まれる」ことも知らないし遺伝子修復機構も持っていないので癌に対しては手も足も出ないのです。何故細胞システムは遺伝子修復機構を持っていないのでしょうか?何故ならばDNA修復機構を支配しているのは遺伝子だからです。このようなすごい遺伝子はいずれ未来の長い長い遺伝子の進化の中での突然変異によって生まれるかもしれません。それまでに人類はAIによって殺されてしまっているかもしれません。アッハッハ!!!
細胞のシステムはDNAの損傷と癌関連遺伝子の損傷を区別できますか?できません。
いいえ、細胞のシステムは一般的に「DNAの損傷」と「癌関連遺伝子の損傷」を区別するようには設計されていません。細胞は、DNAに傷があることを検知すると、その傷の種類に関わらず、同じ「DNA損傷応答(DDR)」という機構を発動させます。この機構はDNA修復、細胞周期の停止、細胞老化、アポトーシス(細胞死)などを引き起こしますが、その損傷が癌化に繋がりやすいか、あるいは癌関連遺伝子に特異的なものであるかまでは判断できないのです。
細胞のDNA損傷応答(DDR)の仕組みはDNA損傷に対する応答であって遺伝子損傷応答ではないのですがDNA損傷応答(DDR)いくつかあります。
1.NA損傷の検知:細胞内にはDNAに傷ができたことを感知するセンサーが存在します。
2.修復機構の起動:損傷が検知されると、DNA修復機構が自動的に働き、DNAの修復を試みます。
3.細胞周期の停止:修復が間に合わない場合や、損傷が重大な場合は、細胞周期の進行を一時的に停止させます。これにより、修復に時間がかけられるようになります。
4.アポトーシスまたは老化:修復が不可能と判断されると、細胞はアポトーシス(プログラム細胞死)を起こして死滅するか、細胞老化状態に入ることで、異常な細胞が蓄積するのを防ぎます。
なぜ細胞のシステムはDNAの損傷と癌関連遺伝子の損傷を「区別できない」のか?
細胞のDNA損傷応答機構は、細胞のゲノムの恒常性を維持するための基本的なシステムであり、特定の種類の損傷(癌関連遺伝子の損傷)だけをターゲットにするように作られていません。
「癌関連遺伝子の損傷」は、特定の遺伝子の機能に異常を引き起こすDNAの損傷の一種であり、その損傷自体が細胞システムにとって直接的な「癌」であると判断するわけではありませんし、できません。
むしろ、細胞は「DNAが傷ついた」という事実にのみ反応し、損傷を修復し、異常な細胞の増殖を防ぐという普遍的なメカニズムを働かせますが遺伝子の損傷に対しては100%無知です。だからがんを治せないのです。
細胞のシステムは、特定の遺伝子配列を直接認識して「これはがん関連遺伝子の損傷だ」と区別することはできません。しかし、損傷の種類、程度、場所に応じて、修復方法やその後の細胞の運命を決定する「DNA損傷応答(DDR)」と呼ばれる仕組みが作動します。 細胞が損傷を処理する仕組み細胞は、損傷そのものの性質や、損傷が引き起こす影響に基づいて、対応を変化させます。 損傷の種類による認識の違いDNAは日常的に、紫外線や化学物質、細胞の代謝過程で発生する活性酸素などによって損傷を受けていますが本当にこのような損傷が癌関連遺伝子を損傷させているかはわかっていないのです。細胞には、損傷の種類(塩基の変質、一本鎖切断、二本鎖切断など)に応じて、複数のDNA修復経路が備わっています。それぞれの修復経路は、損傷のタイプを認識する特定のタンパク質によって開始されます。 がん関連遺伝子に変異が起こる細胞の増殖を促す「がん遺伝子」や、増殖を抑える「がん抑制遺伝子」に修復不能な損傷が起こると、細胞の増殖制御が失われます。がん関連遺伝子に発生した損傷は、細胞の増殖制御という重要な機能に影響を与えるため、他の遺伝子の損傷よりも深刻な結果(がん化)を招くのです。
「DNA損傷応答(DDR)」とは細胞内のDNA損傷に対してDNA修復、細胞周期停止、細胞老化、アポトーシスなどを引き起こす正常な細胞機能です。
DNAは癌関連遺伝子の変異事態を癌遺伝子の変異として判断できますか?
DNAそのものが、がん関連遺伝子の変異を「がん遺伝子の変異」だと判断するわけではありません。これは人間の目や思考による判断です。DNAはただの分子であり、自ら良し悪しを判断する知性はありません。
しかし、生物の細胞には、変異の結果生じる「異常な状態」を検知して対処する仕組みが備わっています。その異常が、細胞をがん化させるかどうかは知ることはできません。
細胞が「異常な状態」を検知する仕組み
細胞は変異そのものを「がん」として認識するのではなく、変異によって生じる機能不全や変化を、複数のシステムで検知します。
DNA損傷応答(DDR)
このシステムは、DNAの二重らせん構造に生じた物理的な損傷(二本鎖切断など)を検知します。
細胞ががん遺伝子やがん抑制遺伝子の変異を「がん」だと判断するわけではありません。あくまで、修復が必要な「損傷」として扱います。
細胞周期チェックポイント
細胞の増殖を制御する「細胞周期」には、DNAの複製が正しく行われているかを確認する関所(チェックポイント)があります。遺伝子変異によって増殖を促進するタンパク質が過剰に作られたり、増殖を抑制するタンパク質が機能不全に陥ったりすると、このチェックポイントが異常を検知して細胞分裂を停止させます。
免疫システム
遺伝子変異の結果、細胞の表面に異常なタンパク質(ネオアンチゲン)が表れることがあります。
免疫システム(特にT細胞)は、この異常を「異物」として認識し、がん細胞を攻撃しようとします。これは間違いです。癌細胞は自己の成分ですから免疫は自己を攻撃できないから免疫は癌細胞に対しては無力なのです。
これも変異そのものを認識しているのではなく、変異によって作られた結果としての異常なタンパク質を敵として認識することはできないのです。
「がん遺伝子」と「がん抑制遺伝子」の変異
細胞は、変異が「がん遺伝子」に起きたか、「がん抑制遺伝子」に起きたかを区別できません。
がん遺伝子の変異:増殖のアクセルが踏みっぱなしになるような機能亢進が起こると、細胞周期の制御システムが異常を検知しますが遺伝子の異常であるとは判断できません。
がん抑制遺伝子の変異:増殖のブレーキが利かなくなるような機能喪失が起こると、DNA損傷応答や細胞周期の制御システムが異常を検知しますが 遺伝子の異常であるとは判断できません。
以上をまとめるとDNAは知性を持たないので、変異を「がん遺伝子」として判断することはありません。しかし、細胞の持つDNA修復システムや細胞周期の制御システム、そして免疫システムは、遺伝子変異によって生じた細胞の異常な振る舞いを検知し、がん化を防ごうと働いているのではなくDNAの損傷であることは認識できますが遺伝子の異常であるとは判断できません。
さて中川恵一先生の間違いだらけの論文の修正を続けます。
突然変異を起こさせる原因として、最大のものはタバコです。と中川先生は長い間言い続けておられます。喫煙が減っているのにもかかわらず癌は増えて行きます。何故でしょうか?喫煙を好む人は煙草がおいしいからではないのです。簡単に説明しますと喫煙を開始して約7秒でニコチンが作用し、イライラ解消が実感されるため、脳で喫煙がよいものだと認識され、ニコチン依存が強化されます。 ただし、ニコチンの影響はなくなるのも早く、イライラやストレスが再び出現します。 これが「ニコチン切れ」という離脱症状(禁断症状)です。「ニコチン切れ」を解消するために再び喫煙を繰り返すのです。タバコの葉に含まれる成分であるニコチンは摂取すると脳の快楽物質であるドーパミンを放出させ、気分が良くなる一方で依存性の原因となります。タバコのストレス解消効果は一時的なもので、むしろニコチン切れによる禁断症状(イライラ、易攻撃性など)を緩和しているにすぎません。 ニコチンの血中濃度の半減期は約30分と短く、喫煙して禁断症状が一時的に解消されても、1日の中で何度もタバコを吸いたくなりイライラなどの症状が出現します。10・7今日はここまで
