何故どのようにして癲癇が起こるのでしょうか?またどうすれば癲癇を治すことができるのでしょうか?答えは極めて簡単で、結論から言うと部分発作であろうが全般発作であろうが癲癇の原因はヘルペスであり脳の大脳基底核に集中している神経細胞体が集まった四つの核(末梢神経の神経節にあたる)に存在する神経細胞に感染したherpesが原因です。大脳基底核は四つの神経核から成り立っています。⑴線条体striatum(尾状核caudate nucleus,被殻putamen)、腹側線条体ventral striatum(腹側 線条体は,側坐核nucleus accumbensを中心に,嗅結節および尾状核・被核の最も腹側部を含む領域)。⑵淡蒼球pallidum,またはglobus pallidus(淡蒼球は 淡蒼球外節external segment of the globus pallidusと,淡蒼球内節internal segment of the globus pallidusと,腹側淡蒼球ventral pallidumから成る)。⑶視床下核subthalamic nucleus。⑷黒質substantia nigra(黒質は黒質網様部substantia nigra pars reticulata,黒質緻密部substantia nigra pars compactaに分かれる)。
大脳基底核のこれら四つの神経核(⑴線条体の尾状核と被殻⑵淡蒼球⑶視床下核⑷黒質)を構成する数多くの脳神経細胞体に感染し、こっそり細胞質から細胞核内に侵入してエンベロープを脱ぎ捨てて環状の遺伝子をむき出しにして隠れて患者の免疫が落ちるまで潜み続け、免疫が落ちたらできる限り多くの自分の遺伝子の複製と増殖を行ったあと細胞質に出てカプシドやテグメントなどを作り、最後は神経細胞の細胞膜をまとってビリオン(子供のウイルス)を完成して次の神経細胞に感染するのです。ヘルペスウイルスのテグメント(あるいはマトリックス)と言われるウイルスタンパク質が20種類あり、その20種類の蛋白の一つに感染直後に宿主細胞のタンパク合成を遮断するタンパク (virion host shut off protein略して(VHS)が存在する。
この時に患者さんの免疫が戻ったり、抗ヘルペス剤を飲むと、増殖の途中で核内での増殖をやめて即座に細胞の核内に隠れ続けようとするのです。ところが免疫が落ちると再び核内で増殖を始めるのです。ひとたび神経細胞に感染して核内に隠れてしまうと人間の免疫は絶対にヘルペスウイルスは殺しきれないので免疫を上げて細胞の核内に潜伏感染に追い込んでヘルペスが自分の遺伝子の複製と増殖をできなくさせるしかヘルペスによる病気を防ぐことはできないのです。ヘルペスウイルスがこの現世に最後に残った病原体の唯一のウイルスであり、人間の免疫が減ったら多種類のスパイク蛋白を持っているのですぐに人体の240種類の組織のあらゆる細胞に感染を広げて、とりわけ中枢神経は免疫が一番弱いので逃げ隠れしやすいので癲癇をはじめとするあらゆる脳疾患を生み出す恐ろしいウイルスとなっているのですが世界中の医者は誰も知らないふりを決め込んでいます。無念ですね。
何故ヘルペスウイルスは人体のすべての細胞に感染できるのでしょうか? すべてのウイルスの中であらゆる点からみて最も進化した天才(?)ウイルスがヘルペスウイルスであるのです。というのはウイルスも遺伝子を持っているので人間と同じ生命体であるので長生きと自分の子供を増やし続けることが唯一のしかも最高のウイルスの目的となります。ところが生命体であるウイルスは細胞に寄生するしか増殖できないので寄生体のあらゆる細胞に感染できればいいのですが、並のウイルスは一種類のスパイク蛋白しかないので一種類の細胞しか感染できないのです。一方ヘルペスウイルスは人体を構成するあらゆる細胞に感染可能なスパイク蛋白を持つウイルスとして進化の頂点に達してしまいました。しかもヘルペスは免疫が最も攻めにくい神経節や神経核の神経ニューロンの神経細胞体に住み家を持つようになったので、寄生体の免疫が落ちたら神経ニューロンを末梢から脳脊髄の中枢まで自由に動き回れるので、最後は脳や脊髄の神経細胞体がいっぱい詰まっている神経核をアジトにしてやりたい放題の狼藉を働き、あらゆる脳脊髄疾患や脳神経変性疾患のすべての原因不明の病気を引き起こしてしまうのです。
さらなるherpesの特技は寄生体の免疫が上がればヘルペスは環状の遺伝子をむき出しにして核内に隠れ続け、免疫が落ちだすと複製増殖するというヒットアンドランの芸当を発揮できるのはherpesウイルスだけなのです。つまり免疫が上がっているときには最高の隠れ家である核内に入り込んで遺伝子を裸にして隠れているherpesを感染細胞は言うまでもなくすべての免疫細胞も抗体もワクチンもherpesの存在さえ気が付かないので手も足も出せないのです。
しかし見方を変えれば免疫を下げない限りは、このように感染細胞の核内にherpesを封じ込めておけば増殖して隣の細胞に感染することができないので免疫に捕まえられることもないのでいつまでもherpesと戦う必要は起こらないのでヘルペスとの戦いによる炎症は一切起こらないのです。つまりherpesによる病気は起こらないので免疫を抑えない限りは絶対に安心と言えます。だからこそ免疫を抑える薬は絶対に使うなと言っているのです。免疫を抑えない限り自己免疫疾患も癲癇もあらゆる難病もすべてなくなってしまうからです。にもかかわらず世界中の医薬業界は朝から晩まで免疫を抑える薬しか作れないので全世界の人間の難病つくりに専念しているのです。世界中の患者さんの苦しみが増えるばかりです。残念です。
まず癲癇発作が起こりやすいのはヘルペスが四つの大脳基底核に感染しているときに免疫が発熱などによって突然に上昇した時に免疫のグリア細胞が感染細胞に潜んでいるヘルペスを見つけ出して攻撃したときに炎症が生じ、さらにその電気信号が伝わる電線である軸索を傷つけるといわばショートが起こり、そのヘルペスとの戦いで生まれた異常な興奮の電気信号が軸索の終末であるシナプスまで伝導していきます。シナプスでは次の新たなるニュ-ロンに情報を伝えるために電気ではなく化学物質であるグルタミン酸などの神経伝達物質に変えて再び異常な興奮の情報を再び電気信号に変えて伝えるのです。最初のヘルペスと炎症細胞であるミクログリアとの戦いで生まれた異常な炎症が生み出した興奮の電気刺激が大脳基底核を構成している多くの次の神経細胞の軸索に伝わり、活動電位が生まれそれらの神経細胞にも同時に異常な活動電位が生じて次々と異常な最初の電気信号が大脳基底核の細胞に伝わり、最終的には大脳新皮質にもこの異常な興奮の電気信号が伝わり、最後は優れた脳でも対応が不可能となり、生命体で最も進化した脳もヘルペスによる炎症性の興奮刺激を処理出来なくなり、仕方なく絶望のあまり癲癇発作を起こさざるを得ないのです。
ここで全身の神経細胞から大脳皮質に伝えられた正常な情報処理と、一方、大脳皮質以外の脳の神経細胞に感染したherpesに対抗する免疫細胞であるミクログリアによる激烈な炎症反応によって生まれた異常電気的興奮の情報処理について、とくに大脳(新)皮質の興奮性シナプス結合と抑制性シナプス結合がどのように癲癇を起こさざるを得ないかに焦点を置いて詳しく説明しましょう。又、何故ヘルペスは大脳皮質の神経細胞には感染したがらないのでしょうか?
大脳皮質には10種類ほどのニューロンがあります。大脳新皮質はヒトが生きて行く上で必要な最高司令官で興奮すべきか抑制すべきかを下します。大脳皮質の神経細胞は興奮性の錐体細胞と、それを抑制性に制御する非錐体細胞の二種類あり、他の皮質領野や皮質下の視床や癲癇にかかわる大脳基底核などの脳の様々な場所からの入力と出力を統合処理し、その複雑な脳の機能を最終的に担っています。本来人間が生きるということは活動するのと同義であり興奮することであり神経を興奮させることです。にもかかわらず脳の興奮を抑制する神経が何故、生まれたのでしょうか?それは普通の人間が興奮して感じる快楽の強さ、興奮の時間的な長さ、興奮の種類、興奮の量には脳が耐えられる限度が必ずあります。というのは脳への興奮は電気信号ですから興奮を高めすぎると脳が受容できる電気量が多くなりすぎて脳のシステムが破壊の恐れがあるので興奮の限界を超えないように脳は自衛するために自然に進化させたのが抑制性の脳神経細胞なのです。ところがヘルペスというとんでもないウイルスがいともたやすく脳神経細胞に感染して炎症による興奮性の刺激を脳に伝えると刺激の強さが普通の生活で見られる興奮とは比較できないほどの興奮は抑制の神経細胞ではどうにもならないので脳の正常な働きの一時的な破綻が癲癇という発作となるのです。抑制性神経細胞とは何でしょうか?
本来人間は生きて快楽の源泉である興奮活動をやるために脳に快楽を興奮として伝えるために興奮性神経がまず進化して生まれたのですが、残念ながら興奮は無限大ですから脳は極めて脆弱でかつ繊細でなによりも脳に存在する「心」が興奮しすぎるとそれこそ癲癇でなくとも心が耐えきれなくて暴発しないように新たなる興奮を抑制する専門の抑制神経細胞が生まれたのです。この新たに進化して生まれた抑制神経を別名、介在神経と呼ばれるようになりました。これからも介在神経はしばしば出てきますが興奮を抑制する神経であることをしっかり覚えてください。特に脳の病気はすべて興奮神経と抑制神経の拮抗のバランスが崩れて生じます。何故バランスが崩れてすべての脳疾患の原因はherpesであるのかを証明するためにこの論文を書いているのです。
大脳皮質では約20%の神経細胞が抑制性神経細胞であり大脳皮質の抑制性神経細胞の大多数は、局所回路において作用することから介在神経細胞(interneuron)とも呼ばれ、興奮性神経細胞からの出力を調整し、出力の同期性を制御したり、過剰興奮を防ぐなど重要な機能をもっているのです。しかしこの介在神経細胞(interneuron)という名称はぴったりしません。もっと適切な名称は局所神経細胞とつけるべきです。何故ならば介在という言葉は「両者の間に他の事物がはさまってあること」ですから介在神経細胞は二つの異なった神経細胞の間に別の神経細胞が挟まるという意味になるからです。実は介在神経は二つの神経に挟まった神経ではなく興奮神経に直接につながった神経であり、興奮を抑える抑制神経であるので敢えて名称をつけるならば「局所抑制神経」が適切だと言えます。本来、介在ニューロンというのはヒトの神経組織で、感覚ニューロンから運動ニューロンへと刺激を伝達する間にある、つまり介在するニューロンのことなのです。また局所ニューロンというと局所の興奮ニューロンも含まれてしまうのでやはり局所抑制ニューロンが混乱を招かないので妥当です。局所の興奮ニューロンは局所興奮ニューロンというべきです。
介在ニューロン(局所抑制ニューロン)は、所属する狭い局所の部位に軸索が限局し、近傍の興奮性神経細胞にのみ情報を伝達するニューロンのことを指すのです。介在ニューロンはほとんどすべてが抑制の役割があり形態学的、電気生理学的、神経化学的な三つの特徴を持っているのでその組み合わせによって多種多様な分類があるのでそれぞれの介在ニューロンが持っている独自の神経化学マーカーだけを取り出して分類が行われています。例えば大脳新皮質では、パルブアルブミン発現細胞、ソマトスタチン発現細胞、その他の抑制性神経細胞の三群に大別することが一般的である。すなわち、① パルブアルブミン(PV)発現細胞、②ソマトスタチン(SOM)発現細胞、③ その他の抑制性神経細胞である。しかしその他にも多くの神経化学マーカーが存在し、実際には様々なサブグループから構成される、複雑な細胞群である。何故このように抑制ニューロンは多様化したのでしょうか?それに対応して抑制の仕方も様々あるからです。この③の他の抑制性神経細胞の代表として今まではカルレチニン(CR)が主要な神経化学マーカーとして長年用いられてきましたが、マウス大脳新皮質では一部のCR発現細胞がSOMをも発現することが明らかにされ、特異的なマーカーとしての有用性が低いことがわかり、最近では血管作動性腸管ペプチド(VIP)が用いられています。こうした化学的分類は、形態学的分類および電気生理学的分類とよく対応しています。
大脳皮質の層構造は1層から6層まであり、各層ごとに特有の入出力構造を持ち、神経細胞は高密度に分布しており、ヒトの大脳皮質には1立方ミリ容積あたり、1万6千個の神経細胞と1億3千万個を超えるシナプス構造があります。1立方ミリ容積あたりにですよ、1万6千個の神経細胞と1億3千万個を超えるシナプス構造があるのを想像できますか!!!!!ニューロンは同じ種類ごとに同じ階層に集まり6層の層構造を作り、このような秩序だった神経回路により情報の伝達はより効率的となり学習、記憶、運動、認知などの高度な情報処理ができるのです。
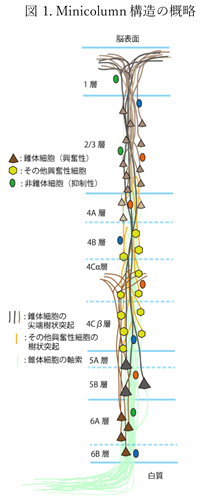
大脳皮質は、解剖学的に、下の図1の「Minicolumn構造の概略」で示したように大脳皮質では縦方向に神経細胞が柱状に並んでおり、ミニ円柱(minicolumn)構造を持ち、80個の神経細胞で構成され、横方向に23μmの幅を持っています。横方向にこのミニ円柱構造が繰り返し分布しています。ミニ円柱構造も横並びの同じ層に同種の機能を持った神経細胞の回路を維持して効率よく素早く同じ情報を伝えるためです。大脳基底核の極めて多くの細胞の密な集団と違って大脳皮質のミニ円柱(minicolumn)構造は興奮性細胞と抑制性細胞が孤立して散在性に存在し神経軸索で連絡しているだけで大脳基底核のさいぼうのようにぎゅう詰めになっているほどではないのです。Herpesが感染したがる大脳の組織は①増殖しやすい細胞体ができる限り多く、しかも②免疫細胞のミクログリアにみつからなくて更に③神経線維である軸索が少ない灰白質の三つの条件を満たす大脳の組織はまさに大脳基底核なのです。一方、大脳の組織でヘルペスが感染したくない組織は大脳白質なのです。何故ならば、大脳白質は神経線維の軸索だけで成り立っているのでヘルペスが住み着いても増殖できる核もないうえに灰白質の細胞体まで長い軸索の距離を頑張って登り切って細胞体まで到着して、そこで増殖しても大脳基底核の細胞ほど子供のビリオンを増やして真横にはない近くの細胞に感染したいと思っても細胞体外に出たらミクログリアに見つけられ食われてしまうので、いつまでも最高の隠れ家でありかつ増殖しやすい、しかも大敵のミクログリアに出会うこともない大脳髄質にある大脳基底核の大量の細胞の細胞体で住み着くようになったのです。大脳基底核の細胞の数は多すぎて誰も数えたことはないのですが、一方、大脳皮質の錐体細胞や非錐体細胞やそのほかの興奮性の細胞を一個ずつ数えことができるくらい少ないのです。

大きくて広い大脳皮質内の局所神経回路はどんな細胞や神経線維からから成り立っているのでしょうか? ①興奮性の錐体細胞、②錐体細胞を取り囲む抑制性の非錐体細胞、そのほかの興奮性細胞などの神経細胞以外に、他の大脳皮質や視床や大脳基底核や大脳辺縁系からの③興奮性入力線維、④中脳の縫線核(raphe nucleus)からのセロトニン線維、⑤マイネルト基底核(basal nucleus)からのアセチルコリン線維、マイネルト基底核は英語でNucleus basalis of Meynert(NBMと省略)は、新皮質へ広く投射する前脳基底部無名質にあるニューロン群である。アセチルコリンとその合成酵素であるコリンアセチルトランスフェラーゼを多く含んでいる。⑥腹側被蓋野(ventral tegmental area略してVTA)からのドパミン線維等の求心性線維等から構成されています。腹側被蓋野(VTA)は辺縁系や大脳皮質へドーパミンを供給する脳部位です。
錐体細胞は、大脳皮質の興奮性出力信号細胞であり、2/3層、5層、6層に分布しています。4層にある興奮性細胞は、主に有棘星状細胞(spiny stellate細胞)や星状錐体細胞(Star pyramid細胞)である。これらの興奮性神経細胞は、層毎に、入力源や出力先が異なる。それらの興奮性出力細胞の活動を抑制性非錐体細胞が抑制性の伝達物質GABAによる作用で抑制し制御する。抑制性非錐体細胞は、1層から6層まで分布しており、形態や発火特性、発現する神経伝達物質の異なるサブタイプが多く存在するのはすでに説明しました。これらの抑制性非錐体細胞のサブタイプは、シナプス結合して抑制作用を及ぼすターゲットの場所が異なり、活動様式も異なる。さらに、外部からの興奮性信号とセロトニン神経である縫線核からの信号や他のそれ以外の活動を調整する信号等が複雑に作用し合うのですが、しかし今なお大脳皮質の働きは眼が眩むほど複雑すぎて解明されていないことが多すぎますがわかっている情報だけを書き連ねて癲癇がどのように起こるのかの説明で用います。
興奮性シナプス結合については、大脳皮質の局所神経回路の興奮性シナプス結合の中では、錐体細胞間のシナプス結合と、視床からの求心性神経線維から錐体細胞へのシナプス結合が興奮性のシナプス結合です。皮質の興奮性細胞間のシナプス結合様式は、4層の興奮生細胞から2/3層の細胞へシナプス結合があり、また4層の興奮性細胞は他の4層の細胞とも結合が強い。さらに4層の興奮性細胞は6層にも少ないながら結合している。2/3層の錐体細胞は、同じ層の中でシナプス結合を作り、5層の錐体細胞に最も強いシナプス結合で信号を送る。5層の錐体細胞は同じ層の錐体細胞と結合し、6層の錐体細胞にも信号を送る。6層の錐体細胞は、4層5層6層の錐体細胞にもシナプス結合する。ややこしいでしょう。
5層の錐体細胞は、対側皮質へ投射するもの投射する交連細胞(commissural cell; COM細胞)と橋核へ行く皮質橋細胞(corticopontine cell; CPn細胞)に分かれる。「投射する」という意味は「神経細胞の軸索が伸びる」ことです。前頭葉の大脳皮質のCOM細胞には、対側線条体にも投射する交差性皮質線条体細胞(crossed-corticostriatal cell; CCS細胞)がある。5層にある錐体細胞投射のサブタイプの間で、樹状突起形態や生理的性質が分化している。そしてこれらサブタイプの組み合わせで、結合方向性、相互結合頻度、短期可塑性が異なっている。神経の可塑性とは何でしょうか?神経系は外界の刺激などによって常に機能的、構造的な変化を起こしており、この性質を一般に“可塑性”と呼んでいる。神経の可塑性は大きく3つに分けられる。1つ目は脳が発生していく時や発達していく段階にみられる可塑性。2つ目は老化や障害を受けた時などに神経の機能単位が消失するが、それが補填・回復されていく場合。3つ目は記憶や学習などの高次の神経機能が営まれるための基盤となっているシナプスの可塑性(synaptic plasticity)である。特に神経科学にとっては3つ目のシナプスの可塑性(synaptic plasticity)が重要で、例えば記憶には、短期記憶と長期記憶があるが、短期記憶は主にシナプスでの伝達効率の変化により、長期記憶はシナプス結合の数や形態の変化により達せられるのです。このように複雑な機能と神経回路で結びついている脳の大脳基底核に莫大な数の神経細胞に感染したherpes感染が免疫が落ちた時に増殖して細胞外に出た時に免疫の王者であるミクログリアに見つかり貪食されたり戦いが始まれば炎症反応が出現して異常な信号が一挙にあらゆる細胞に伝わると意識も記憶もすべて失う癲癇発作が起こるのです。
一方、視床皮質神経線維を選択的に発現する小胞型グルタミン酸トランスポーター Type 2 (vesicular glutamic transporter type 2 略してVGLUT2)をマーカーとして使うことで、視床由来神経線維の神経末端の皮質内分布と皮質細胞への結合様式が明らかとなり前頭葉では、1層上部、4層、5層下部(5b層)に、より多くの視床皮質線維の神経末端が分布していることがわかり、その神経終末の大半は錐体細胞の樹状突起の棘突起に入力し、その棘突起の1割には抑制性シナプスが同時に入力し、視床からの皮質に投射される興奮性信号を選択的に抑制して皮質に有害な興奮が伝わらなくしているのですがヘルペスの天才ぶりには人間の免疫システムは勝てないのです。
それでは脳内の神経細胞(ニューロン)はどのようにしてシナプスを介して数多くの神経細胞を結び付けて脳に神経回路を作れるのでしょうか?復習しましょう。
神経軸索の末端であるシナプス前終末から放出された神経伝達物質は、シナプス硬膜の受容体に結合してシナプス電位を発生させます。シナプス電位には、膜電位を脱分極の方向へシフトさせる興奮性と、過分極方向へシフトさせる抑制性の二つがありますがしっかり頭に入れてもらいたいのは興奮する神経と興奮を抑制する介在性神経とは別の神経であることです。
興奮性シナプス電位を発生させる代表的な神経伝達物質がグルタミン酸であり、抑制性のシナプス電位を発生させる代表的な神経伝達物質がγアミノ酪酸(GABA)です。グルタミン酸を出す神経とγアミノ酪酸(GABA)を出す神経は別の神経ですよ。あるニューロンにおいて興奮性シナプス電位がいくつか足されてある大きさの閾値を超えると活動電位が発生し、これを発火と言います。癲癇の場合は、興奮性シナプス電位がいくつか生まれ積算されると大きくなりすぎて大きさの閾値をはるかに超えすぎてしまうので爆発的な活動電位が発生しいわゆるショートが起こり癲癇の全般大発作がおきてしまうのです。
正常な活動電位ではその発火と言われる活動電位はニューロンの軸索を伝わり、そのシナプス前終末まで伝わり、再びそのシナプス前終末から伝達物質を放出し、次のニューロンにシナプス電位を発生させる。そして、一方、別の神経の抑制性シナプス電位は興奮性シナプス電位を生み出した影響を止める方向に働くのです。
大脳皮質領域の神経回路はグルタミン酸を興奮性伝達物質として用い脳内の離れた領域へ軸索投射をする興奮性の錐体ニューロンと、もう一つは近隣のニューロンへGABAを介した抑制性シナプスを錐体ニューロンと形成する介在抑制ニューロンによって構成されているのです。以上のように大脳皮質の神経細胞シナプスの興奮の連絡と抑制の連絡は分かっているのですがそのどんな興奮にさいしてどのように、何故な抑制がかかるのはヘルペスとの戦いかという意味付けはほとんど何も知られていないのです。言うまでもなくヘルペスとの戦いはヘルペスは絶対に殺しきれないので無駄な戦いはやめなさいという警告が介在抑制ニューロンの最も大切な役割とも言えます。しかしherpesには永遠にだからこそすべての病気の原因は免疫を抑える対症療法で増やしたherpesには勝てないのです。
抑制性シナプス結合についてはGABAを伝達物質とする抑制性非錐体細胞には少なくとも十数種類のサブタイプがあり、それぞれ異なった役割で皮質活動を制御する。主な抑制性非錐体細胞は1)バスケット細胞2)シャンデリア細胞3)マルチノッチ細胞4)ダブルブーケ細胞5)ニューログリアフォーム細胞6)水平軸索結合の6種類があります。それぞれの抑制性非錐体細胞について説明します。
1)バスケット細胞(籠細胞)は最も多数をしめるサブタイプであり、急速活動電位を示すfast spiking (FS)型の発火様式で非錐体細胞の3割をしめる集団で、互いに一般の化学結合ではなくギャップ結合と言われる電気シナプスで結合し、イオンチャンネル型の化学結合によるシナプス結合ではないのです。錐体細胞等の細胞体や樹状突起の細胞体近位部に抑制性シナプスを形成し、錐体細胞の発火を押さえたり、発火のタイミングの制御をするのです。バスケット細胞(籠細胞)の軸索が標的細胞の細胞体をバスケット状に取り囲むことからバスケット細胞と命名された。
2)シャンデリア細胞も、もう一つの抑制性非錐体細胞サブタイプでありバスケット細胞と同じく急速活動電位を示す急速活動電位型のFS型発火様式です。シャンデリア細胞の数は少ない。その神経軸索終末は縦方向に10個程度が数珠状に並び、ほぼ全ての錐体細胞の軸索起始部にシナプス結合し、錐体細胞の発火を強く制御する。FS細胞は、ほぼ全てがカルシウム結合タンパク質パルブアルブミン(parvalbumin)を発現している。シャンデリアの名前の由来は多くの電球に似たシャンデリアの様に明るく発火するように飾られているのでシャンデリア細胞と名付けられた神経細胞の神経終末は縦方向に10個程度が数珠状に並び、ほぼ全ての錐体細胞の軸索起始部にシナプス結合し、錐体細胞の発火を強く制御するのでつけられたのです。
3)マルチノッチ細胞は2番目に多い抑制性非錐体細胞のサブタイプで神経ペプチドソマトスタチン(somatostatin)を発現するマルチノッチ細胞(Martinotti細胞)である。マルチノッチ細胞は大脳皮質の第II層~第VI層に細胞体を有するGABA作動性の抑制性のニューロンです。Martinotti細胞の意味は形が多極性紡錘形の神経細胞であるからです。非錐体細胞の中では唯一高密度の棘突起(約1個/µm)を持ち、軸索は、1層まで分岐しながら伸展し、錐体細胞の樹状突起等の末端の樹状突起にもシナプスを作り、興奮性入力信号を直接抑制する。
4)ダブルブーケ細胞は3番目に多い抑制性非錐体細胞のサブタイプでダブルブーケ細胞(Double bouquet細胞)と呼ばれているのはブーケ(花束)の様に、軸索がまとまって花束の様に束となり白質方向に下降するのが特徴であるからです。カルシウム結合タンパク質のカルレチニン(calretinin)や神経ペプチドVIP、CRF等を発現する。結合のターゲットには錐体細胞に加えてdouble bouquet細胞を含む非錐体細胞も含まれる。
5)ニューログリアフォーム細胞は遅速発火(Late spiking)特性を持ち、ニューログリアフォーム細胞と名称されたのは突起を多く持って周辺に張り巡らしているグリア細胞に似て軸索を細胞体の近傍に蜘蛛の巣状に張り巡らしているからです、このニューログリアフォーム細胞の状突起や軸索は、自身の細胞体近傍に密に分岐している。長い抑制効果を示す抑制性のGABAB受容体反応を後シナプス細胞に引き起こす。
6)水平軸索結合は、同じ方向選択性を持つ機能円柱(orientation column)同士をつなぐ役割を持っている。皮質領域内に機能しない部位ができた際にすぐに代償の信号ルートを作る為の予備的な回路の役割を水平軸索が持つ。
物凄く物凄く物凄く!!詳しく書きすぎたので分割します。続きはこちらです!!難しいですが着いて来て下さい!!
